
ABSTRAK
Studi ini bertujuan untuk menilai dampak suplementasi Ganoderma lucidum (200–11.200 mg/hari, 1–24 minggu) terhadap indeks terkait kesehatan pada populasi termasuk individu yang sehat, berisiko, dan penderita penyakit kronis. Tinjauan sistematis dan meta-analisis dilakukan dengan menggunakan data dari EMBASE, PubMed, Web of Science, dan Scopus hingga Agustus 2024. Analisis gabungan dari 17 uji coba terkontrol acak (RCT) yang melibatkan 971 peserta mengungkapkan bahwa suplementasi Ganoderma lucidum menunjukkan pengurangan yang signifikan dalam indeks massa tubuh (BMI) (Weighted Mean Difference [WMD] = -0,43; 95% Confidence Interval [CI]: -0,77, -0,10; p = 0,011), kreatinin (WMD = -0,14; 95% CI: -0,27, -0,02; p = 0,028), glutathione peroksidase (GPx) (WMD = 2,29; 95% CI: 1,67, 2,92; p < 0,001), dan denyut jantung (HR) (WMD = -3,92; 95% CI: -7,45, -0,40; p = 0,029). Tidak ada efek signifikan yang diamati pada lemak tubuh, lingkar pinggang, tekanan darah, glukosa puasa, profil lipid, penanda inflamasi, atau enzim hati. Analisis subkelompok menunjukkan efek bervariasi menurut kondisi kesehatan, dosis, durasi, dan usia. Analisis subkelompok mengungkapkan variasi efek suplementasi Ganoderma berdasarkan kondisi kesehatan, dosis, durasi intervensi, usia saat intervensi, negara, ukuran sampel, dan tahun publikasi. Perbaikan signifikan diamati pada BMI, TC, kreatinin, dan MDA pada subkelompok tertentu, seperti mereka yang menerima dosis lebih rendah (<1400 mg/hari) atau mereka yang berusia <50 tahun. Profil GRADE untuk suplementasi Ganoderma mengevaluasi kepastian hasil dan menunjukkan bahwa kualitas bukti sangat rendah di semua hasil. Suplemen Ganoderma lucidum mungkin memiliki efek sederhana pada indeks kesehatan tertentu, tetapi buktinya dibatasi oleh kualitas yang sangat rendah.
Singkatan
AKSES
asetil-CoA karboksilase
ACOX1
asil-CoA oksidase 1
AFib
fibrilasi atrium
ALT
alanin aminotransferase
API
bahan aktif farmasi
Bahasa Inggris
aspartat aminotransferase
Bf
lemak tubuh
Indeks Massa Tubuh (IMT)
indeks massa tubuh
BP
tekanan darah
Penyakit Jantung Koroner (PJK)
penyakit jantung koroner
CI
interval kepercayaan
Bahasa Indonesia: CMC
Kimia, Manufaktur, dan Kontrol
Bahasa Inggris: CMS
sindrom kardiometabolik
Bahasa Indonesia: CRP
Protein C-reaktif
Penyakit kardiovaskular
penyakit kardiovaskular
Bahasa Inggris
buta ganda
DBP
tekanan darah diastolik
DNA
asam deoksiribonukleat
Badan Pengawas Obat dan Makanan (BPOM)
Badan Pengawas Obat dan Makanan Amerika Serikat
FPG
glukosa plasma puasa
FRAP
kemampuan reduksi besi plasma
GPx
glutation peroksidase
HbA1c
hemoglobin A1c
HDL-C
kolesterol lipoprotein densitas tinggi
HFD
diet tinggi lemak
hs-CRP
protein C-reaktif sensitivitas tinggi
Tekanan darah tinggi
hipertensi
Pesawat IL-6
interleukin-6
LDL-C
kolesterol lipoprotein densitas rendah
MDA
malondialdehida
MetS
sindrom metabolik
komputer
terkontrol plasebo
PRISMA
item pelaporan yang disukai untuk tinjauan sistematis dan meta-analisis
KESEJAHTERAAN
daftar prospektif internasional tinjauan sistematis
R
diacak
Bahasa Inggris
artritis reumatoid
Uji coba terandomisasi (RCT)
uji coba terkontrol acak
SBP
tekanan darah sistolik
MERUMPUT
superoksida dismutase
Diabetes tipe 2
diabetes melitus tipe 2
TC
kolesterol total
Tg
trigliserida
TNF-α
faktor nekrosis tumor alfa
Toilet umum
Lingkar pinggang
SIAPA
Organisasi Kesehatan Dunia
WHR
rasio pinggang-pinggul
Senjata pemusnah massal
perbedaan sapih tertimbang
1 Pendahuluan
Penyakit kardiovaskular (PKV) memiliki implikasi yang mendalam bagi masyarakat, ekonomi, dan kesejahteraan individu. Menurut Organisasi Kesehatan Dunia (WHO), PKV menyebabkan sekitar 17 juta kematian di seluruh dunia setiap tahunnya (Organisasi WH 2011 ). Di antara manifestasinya, penyakit jantung koroner (PJK) merupakan kontributor utama terhadap mortalitas di seluruh dunia, sementara stroke tetap menjadi penyebab utama kecacatan di banyak negara (Organisasi WH 2011 ). Dengan meningkatnya prevalensi diabetes dan obesitas di negara-negara industri dan berkembang, tingkat morbiditas dan mortalitas terkait PKV diperkirakan akan menunjukkan peningkatan yang bersamaan (Capewell et al. 2010 ; Hossain et al. 2007 ; Rahimlou et al. 2022 ).
Etiologi CVD mencakup banyak faktor. Para ilmuwan telah mengidentifikasi lebih dari 300 variabel yang mungkin terkait dengan perkembangan penyakit vaskular, dengan hubungan timbal baliknya yang berpotensi menyebabkan konsekuensi metabolik yang kompleks. Determinan risiko utama yang dapat dimodifikasi meliputi penggunaan produk tembakau, asupan alkohol, hipertensi (HTN), peningkatan lipid, glukosa darah tinggi, dan berat badan berlebih. Faktor risiko yang dapat dimodifikasi, termasuk penggunaan tembakau, konsumsi alkohol, hipertensi, dislipidemia, hiperglikemia, dan obesitas, berkontribusi secara signifikan terhadap beban CVD (Capewell et al. 2010 ; Hossain et al. 2007 ; Rahimlou et al. 2022 ). Penelitian terbaru juga menyoroti biomarker yang muncul karena potensinya dalam memprediksi dan memahami patogenesis CVD, termasuk kadar homosistein, indikator inflamasi seperti protein C-reaktif (CRP), dan penanda koagulasi seperti fibrinogen (Pearson et al. 2003 ).
Senyawa herbal telah menunjukkan hasil yang menjanjikan dalam mengelola faktor risiko penyakit kardiovaskular, dengan beberapa menunjukkan efek positif (Vahdat et al. 2020 ; Morshedzadeh et al. 2021 ; Morvaridi et al. 2020 ). Namun, uji coba sebelumnya pada Ganoderma lucidum dibatasi oleh ukuran sampel yang kecil, metodologi yang tidak konsisten, dan formulasi suplemen yang bervariasi, sehingga memerlukan sintesis bukti yang komprehensif.
Selama lebih dari 2000 tahun, Ganoderma lucidum ( G. lucidum ), yang secara tradisional dikenal sebagai “lingzhi” atau “reishi,” telah dihargai dalam pengobatan Asia dan baru-baru ini menarik perhatian dalam praktik medis Barat. Jamur ini menempati posisi unik sebagai agen terapeutik dan nutrisi, dikaitkan dengan sifat-sifat yang dapat mendukung pemeliharaan kesehatan, memperpanjang umur, dan mengatasi berbagai kondisi sistemik (Willard 1990 ). Minat penelitian pada G. lucidum telah tumbuh karena kemampuannya yang terbukti untuk memengaruhi beberapa faktor risiko CVD dengan aman. Sementara metode persiapan tradisional seperti rebusan, teh, dan kopi tetap tersedia, pasar Barat semakin menyukai ekstrak standar dalam bentuk tablet dan kapsul. Organisme ini terdiri dari tiga komponen utama: tubuh buah (basidiokarp), miselium (struktur seperti benang), dan spora reproduksi. Komponen bioaktifnya meliputi berbagai senyawa termasuk polisakarida (terutama beta-D-glukan, heteropolisakarida, dan glikoprotein), triterpen, germanium, asam amino (baik esensial maupun nonesensial), sterol, lipid, antioksidan, vitamin B kompleks (B1, B2, dan B6), dan mineral termasuk zat besi, kalsium, dan seng. Senyawa bioaktifnya, termasuk polisakarida (misalnya, beta-D-glukan) dan triterpen, dihipotesiskan memiliki efek terapeutik. Polisakarida dapat mengurangi stres oksidatif dengan meningkatkan aktivitas enzim antioksidan, seperti glutation peroksidase (GPx), dan memodulasi peradangan melalui interaksi reseptor Toll-like (TLR) (Huie dan Di 2004 ). Triterpen dapat menurunkan tekanan darah (BP) dengan menghambat enzim pengubah angiotensin (ACE) dan memperbaiki profil lipid melalui peningkatan antioksidan (Huie dan Di 2004 ; McKenna et al. 2012 ).
Senyawa-senyawa ini diyakini mendukung potensi terapeutik G. lucidum , khususnya terkait kesehatan kardiovaskular dan metabolik. Misalnya, beta-D-glukan, kelas polisakarida utama, telah terbukti memodulasi respons imun dan mengurangi peradangan sistemik dengan berinteraksi dengan TLR dan menekan sitokin pro-inflamasi seperti tumor necrosis factor-alpha (TNF-α) dan Interleukin-6 (IL-6), yang sangat penting dalam patogenesis aterosklerosis dan resistensi insulin (Klupp et al. 2015 ). Triterpen, konstituen utama lainnya, menunjukkan efek antihipertensi potensial melalui penghambatan aktivitas ACE dan pengurangan stres oksidatif melalui peningkatan enzim antioksidan seperti superoksida dismutase (SOD) dan katalase, sehingga berkontribusi pada peningkatan profil lipid dan fungsi vaskular (Abdullah 2018 ). Hasil dalam tinjauan ini dipilih berdasarkan relevansinya dengan kesehatan kardiovaskular dan metabolisme, didukung oleh bukti praklinis yang menunjukkan efek Ganoderma pada stres oksidatif, peradangan, dan metabolisme lipid (Klupp et al. 2015 ; Abdullah 2018 ).
Investigasi klinis telah mengungkap kapasitas G. lucidum untuk menurunkan tekanan darah, kolesterol, dan kadar glukosa (Gao, Chen, et al. 2004 ; Gao, Lan, et al. 2004 ; Kanmatsuse et al. 1985 ; Jin et al. 1996 ; Wachtel-Galor, Tomlinson, et al. 2004 ). Studi-studi ini tidak melaporkan efek samping pada penanda fungsi hati atau ginjal, dan peserta tidak mengalami reaksi samping yang signifikan. Sementara protokol pemberian dosis optimal masih belum terstandarisasi, rekomendasi saat ini umumnya menyarankan konsumsi ekstrak kering harian antara 1,5 dan 9 g (Chang dan Miles 2004 ; Soo 1996 ). Meskipun beberapa sumber menyarankan peningkatan potensi dalam sediaan spora, validasi ilmiah dari klaim ini dan implikasi terapeutiknya masih tertunda.
Untuk mengatasi kesenjangan kritis ini dalam literatur, dan mengingat pentingnya tinjauan sistematis dan meta-analisis RCT dalam pengambilan keputusan klinis, penelitian ini dilakukan untuk memberikan tinjauan sistematis yang dinilai Grading of Recommendations Assessment, Development and Evaluation (GRADE) dan meta-analisis dosis-respons dari uji klinis. Kami mengevaluasi RCT secara sistematis untuk menyelidiki hubungan antara faktor-faktor seperti dosis Ganoderma dan durasi pengobatan dan berbagai parameter kesehatan. Tujuan dari penelitian ini adalah untuk mengevaluasi secara sistematis efek nutrisi dan terapi G. lucidum pada kesehatan manusia, dengan fokus khusus pada dampaknya pada hasil kardiovaskular dan metabolik, melalui penerapan tinjauan sistematis yang ketat dan metodologi meta-analisis dosis-respons yang memanfaatkan kerangka kerja GRADE. Dengan memeriksa data dari RCT, temuan kami bertujuan untuk memberikan wawasan yang berharga dan berbasis bukti untuk rekomendasi klinis dan kesehatan masyarakat, yang menekankan peran potensial Ganoderma dalam pencegahan dan pengelolaan penyakit kardiovaskular dan metabolik.
2 Metode
2.1 Protokol dan Registrasi
Tinjauan sistematis dan metaanalisis ini dilakukan menurut protokol yang telah ditetapkan sebelumnya yang selaras dengan pedoman Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) 2020 untuk memastikan ketelitian metodologis dan transparansi di seluruh proses (Moher et al. 2015 ). Protokol penelitian ini didaftarkan dalam International Prospective Register of Systematic Reviews (PROSPERO), sebuah basis data internasional untuk tinjauan sistematis, dengan pengenal unik CRD42025632414.
2.2 Pencarian Literatur dan Pemilihan Studi
Kami melakukan penelusuran menyeluruh di sejumlah basis data elektronik utama: MEDLINE (melalui PubMed), Scopus, EMBASE, Cochrane Library, dan Web of Science, tanpa batasan terkait bahasa artikel atau bahasa pelaporan, hingga Agustus 2024. Artikel diidentifikasi melalui penelusuran manual pada daftar referensi publikasi yang diambil dan artikel tinjauan terkait lainnya. Tinjauan difokuskan pada studi yang secara langsung melaporkan RCT yang meneliti efek suplementasi dengan G. lucidum pada hasil terkait kesehatan.
Metodologi pencarian disesuaikan dengan masing-masing basis data, dengan menggabungkan terminologi penting termasuk “ Ganoderma lucidum ,” “Reishi,” dan “uji klinis,” sesuai dengan terminologi MeSH dan kata kunci EMTREE yang relevan (Tabel S1 ).
2.3 Kriteria Inklusi/Eksklusi dan Ekstraksi Data
Studi yang memenuhi syarat adalah uji coba terandomisasi (RCT) yang melibatkan peserta manusia berusia ≥ 18 tahun, yang membandingkan suplementasi Ganoderma lucidum (misalnya, ekstrak, bubuk spora, kapsul, atau tablet) dengan kelompok kontrol dan melaporkan hasil yang berkaitan dengan kesehatan. Tidak ada durasi intervensi minimum yang ditetapkan untuk memastikan tinjauan yang komprehensif. Kriteria eksklusi meliputi studi hewan/in vitro, desain non-RCT, dan studi yang tidak memiliki data yang cukup untuk perhitungan ukuran efek.
Dua peneliti independen (AJ dan HM) melakukan penyaringan awal judul dan abstrak untuk menentukan relevansi studi. Publikasi terpilih kemudian menjalani evaluasi teks lengkap yang komprehensif untuk mengonfirmasi kelayakannya untuk dimasukkan. Dalam kasus di mana konsensus tidak dapat dicapai, peninjau ketiga (BA) diajak berkonsultasi untuk menyelesaikan perbedaan. Tim peneliti menggunakan EndNote versi 7.0 untuk organisasi referensi dan penghapusan entri duplikat. Ekstraksi data dilakukan sesuai dengan templat yang telah ditetapkan sebelumnya yang menangkap informasi utama termasuk karakteristik studi, demografi peserta, spesifikasi intervensi, dan hasil yang dilaporkan.
Dalam uji coba crossover, data secara eksklusif diambil dari periode perawatan pertama untuk meminimalkan potensi efek carryover. Ketika periode washout yang memadai dan penyesuaian untuk variabilitas intra-subjek dilaporkan, perbedaan rata-rata berpasangan digunakan. Sebaliknya, penelitian tanpa penyesuaian tersebut dianalisis sebagai uji coba kelompok paralel.
2.4 Penilaian Kualitas dan Pemeringkatan Bukti
Untuk mengevaluasi ketelitian metodologis, kami menggunakan alat Cochrane Risk of Bias 2.0 (Higgins et al. 2011 ). Dua peninjau (AJ dan ZM) secara independen melakukan penilaian kualitas dengan memeriksa beberapa domain metodologis: prosedur pengacakan, metode penyembunyian alokasi, protokol penyamaran, kelengkapan data hasil, dan potensi bias pelaporan. Ketika perbedaan evaluatif muncul di antara peninjau, penyelesaian dicapai melalui diskusi kolaboratif atau arbitrase oleh peninjau ketiga (BA).
Evaluasi kepastian bukti mengikuti metodologi kerangka GRADE, yang mengkategorikan kualitas bukti sebagai tinggi, sedang, rendah, atau sangat rendah. Penilaian sistematis ini menggabungkan beberapa kriteria evaluatif, termasuk desain penelitian, konsistensi hasil, ketepatan temuan, keterarahan bukti, dan implikasi bias publikasi yang potensial.
2.5 Analisis Statistik
Perhitungan meta-analitik dilakukan menggunakan Stata versi 15.0 (StataCorp, College Station, Texas). Analisis tersebut menggabungkan data pra- dan pasca-intervensi, termasuk rata-rata, deviasi standar, dan jumlah peserta, dari RCT yang memenuhi syarat. Untuk penelitian yang tidak memiliki ukuran statistik langsung, data yang hilang diestimasikan menggunakan rumus standar atau diminta dari penulis jika memungkinkan. Ukuran efek gabungan dihitung menggunakan perbedaan rata-rata tertimbang (WMD) disertai dengan interval kepercayaan 95% (CI) yang sesuai untuk perbandingan lintas penelitian.
Model efek acak diterapkan dengan menggunakan metode DerSimonian dan Laird untuk memperhitungkan variabilitas di antara berbagai penelitian. Pemilihan model efek acak didasarkan pada heterogenitas yang diantisipasi di antara berbagai penelitian yang disertakan, mengingat adanya perbedaan dalam populasi, protokol intervensi, dosis, dan pengukuran hasil. Model ini tidak hanya mempertimbangkan kesalahan pengambilan sampel dalam penelitian tetapi juga memasukkan variabilitas antar-penelitian, sehingga menghasilkan estimasi gabungan yang lebih konservatif dan dapat digeneralisasi. Adanya heterogenitas klinis dan metodologis yang substansial semakin membenarkan pendekatan ini.
Heterogenitas statistik dievaluasi menggunakan statistik I2 , dengan ambang batas 25%, 50%, dan 75% ditafsirkan sebagai indikasi heterogenitas rendah, sedang, dan tinggi.
Untuk studi di mana ukuran statistik langsung tidak tersedia, data yang hilang diestimasi menggunakan rumus mapan yang direkomendasikan dalam literatur. Secara khusus, ketika studi melaporkan kesalahan standar alih-alih deviasi standar (SD), SD dihitung menggunakan rumus: SD = SE × sqrt ( n ), di mana n menunjukkan ukuran sampel. Dalam kasus di mana studi menyediakan median bersama dengan rentang atau rentang interkuartil (IQR), kami menerapkan metode yang dijelaskan oleh Hozo et al. (Hozo et al. 2005 ) dan Wan et al. (Wan et al. 2014 ) untuk memperkirakan mean dan SD. Selain itu, untuk studi yang hanya melaporkan hasil pra dan pasca intervensi tanpa SD perubahan, SD perubahan dihitung menggunakan: (SD = akar kuadrat [(SD pra-perawatan) 2 + (SD pasca-perawatan) 2 − (2R × SD pra-perawatan × SD pasca-perawatan)]) dengan koefisien korelasi yang diasumsikan R sebesar 0,5 tanpa adanya nilai yang dilaporkan. Pendekatan ini memastikan konsistensi dan ketahanan dalam perhitungan meta-analitik kami.
Analisis subkelompok dikelompokkan berdasarkan kondisi kesehatan (kondisi penyakit kronis termasuk sindrom kardiometabolik (CMS), penyakit jantung koroner berisiko tinggi, hipertensi/dislipidemia, diabetes melitus tipe 2 (T2DM) & sindrom metabolik, asma, fibrilasi atrium (AFib), artritis reumatoid (RA), dan angina pektoris stabil; individu berisiko tetapi umumnya sehat, termasuk mereka yang kelebihan berat badan, obesitas, menunjukkan disfungsi hati ringan, memiliki dislipidemia, dan subjek lanjut usia; dan kondisi sehat yang mencakup individu sehat, mereka yang memiliki kesehatan umum yang baik, dan subjek yang bebas dari penyakit neurodegeneratif), dosis Ganoderma (≤ 1400 mg/hari vs. > 1400 mg/hari), durasi intervensi (≤ 8 minggu vs. > 8 minggu), usia (≤ 50 tahun vs. > 50 tahun), wilayah geografis (Asia Timur, termasuk Tiongkok, Hong Kong, Taiwan, dan Indonesia; Timur Tengah, termasuk Israel dan Iran; dan wilayah yang mencakup Amerika, Oseania, dan Eropa, termasuk AS, Australia, Brasil, dan Spanyol), ukuran sampel (≤ 40 vs. > 40 peserta), dan tahun publikasi (≤ 2019 vs. > 2019). Meta-regresi tidak dilakukan karena terbatasnya jumlah studi per hasil (< 10), sesuai dengan pedoman Cochrane.
Analisis pengaruh dilakukan untuk menilai dampak setiap studi terhadap temuan keseluruhan. Adanya bias publikasi diperiksa menggunakan uji Egger dan Begg.
3 Hasil
3.1 Pemilihan Studi
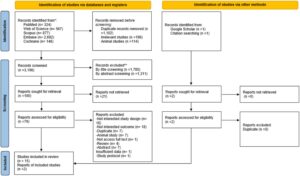
Proses pemilihan studi diilustrasikan dalam Gambar 1. Sebanyak 4608 studi diidentifikasi melalui pencarian basis data: PubMed ( n = 324), ISI Web of Science ( n = 567), Scopus ( n = 877), Embase ( n = 2692), dan Cochrane Library ( n = 148). Setelah penghapusan duplikat ( n = 1102), studi yang tidak relevan ( n = 196), dan studi hewan ( n = 114), 3196 studi disaring berdasarkan judul dan abstrak. Dari jumlah tersebut, 3117 dikecualikan, sehingga menghasilkan 79 studi teks lengkap yang menjalani evaluasi lebih lanjut. Enam puluh empat studi dikecualikan karena tidak melaporkan hasil yang diinginkan, seperti yang dirinci dalam Tabel S2 . Akibatnya, 17 studi yang terdiri dari 971 partisipan dimasukkan dalam tinjauan sistematis dan meta-analisis.
3.2 Karakteristik Studi
Karakteristik studi yang disertakan dirangkum dalam Tabel 1. WMD dan 95% CI untuk perubahan indeks massa tubuh (BMI), lemak tubuh (BF), lingkar pinggang (WC), berat, rasio pinggang-pinggul (WHR), tekanan darah diastolik (DBP), tekanan darah sistolik (SBP), glukosa puasa, protein C-reaktif sensitivitas tinggi (hs-CRP), TNF-α, kolesterol lipoprotein densitas tinggi (HDL-C), kolesterol lipoprotein densitas rendah (LDL-C), kolesterol total (TC), trigliserida (TG), alanine aminotransferase (ALT), aspartate aminotransferase (AST), kreatinin, kemampuan reduksi besi plasma (FRAP), glutation peroksidase (GPx), malondialdehid (MDA), SOD, dan denyut jantung (HR) ditunjukkan dalam Gambar S1–S8 ; plot corong untuk hasil ini disajikan dalam Gambar S9 .
| Tahun studi (Ref.) | Negara | Desain studi | Kondisi kesehatan | Ukuran sampel (Jenis kelamin) | Ukuran sampel (INT/CON) | Durasi percobaan (Minggu) | Rata-rata usia & BMI (INT/CON) | Dosis suplemen (mg/hari) | Jenis suplemen (INT/CON) | Hasil |
|---|---|---|---|---|---|---|---|---|---|---|
| Wachtel-Galor, Tomlinson, dkk. ( 2004 ) | Cina | PC, DB, lintas | Sehat | 36 (NR) | Tanggal 18/18 | 4 | Usia: 32 ± 10/32 ± 10
BMI: Tidak |
tahun 1440 | Kapsul: Ganoderma lucidum (Lingzhi)/Placebo
Diminum dengan 200–400 mL air hangat |
FRAP, TC, TG, HDL-C, LDL-C, hs-CRP, SOD, GPx, MDA, ALT, AST dan Kreatinin |
| Wachtel-Galor, Szeto, dkk. ( 2004 ) | Cina | PC, DB, lintas | Sehat | 10 (B) | 5/5 | 1 | Usia: 32,5 ± 10,4/32,5 ± 10,4
BMI: 22,6 ± 2,6 |
720 | Kapsul: Ganoderma lucidum (Lingzhi)/Placebo | FRAP, TC, TG, HDL-C, LDL-C, LDL-C/HDL-C, SOD, GPx dan MDA |
| Wen dkk. ( 2005 ) | Cina | R, Komputer, DB | Asma alergi sedang-berat | 91 (B) | 45/46 | 4 | Usia: 44,6 ± 11,3/45,1 ± 12,0
BMI: Tidak |
3600 | Kapsul: ASHMI (mengandung Ganoderma lucidum ) + Plasebo yang tampilannya mirip dengan prednison/Prednison + plasebo ASHMI | IL-5, IL-13 dan IFN-γ |
| Li dan kawan-kawan ( 2007 ) | Hongkong | R, Komputer, DB | Bahasa Inggris | 58 (B) | Tanggal 28/30 | 24 | Usia: 50 ± 10/50 ± 13
BMI: Tidak |
11.200 | Kapsul: Ganoderma lucidum (Lingzhi) & San Miao San (SMS) yang mengandung ekstrak G lucidum, Rhizoma atractylodis (Cangzhu), Cotex phellodendri (Huangbai), dan Radix achyranthes Bidentatae (Niuxi)/Placebo | ESR, CRP dan FRAP |
| Kelly-Pieper dan kawan-kawan ( 2009 ) | Amerika Serikat | R, Komputer, DB | Asma | 20 (B) | 12/8 | 1 | Usia: 32 ± 7/31 ± 9
BMI: Tidak |
tahun 1200 | Kapsul: ASHMI [(Ling-Zhi ( Ganoderma lucidum ), Ku-Shen ( Sophora flavescens ), dan Gan-Cao (Glycyrrhiza uralensis))]/Placebo (tepung maizena) | IL-1ra, IL-3, IL-9, IL-12 (P40), IL-13, IL-18, IFN-γ, ICAM-1, VCAM-1, Glukosa, Kreatinin, ALT & AST |
| Chu dan kawan-kawan ( 2012 ) | Hongkong | R, PC, DB, Silang | Hipertensi dan/atau dislipidemia | 23 (B) | 13/10 | 12 | Usia: 56 ± 9,3/53,2 ± 6,7
BMI: 26,1 ± 4,90/26,8 ± 3,9 |
tahun 1440 | Kapsul: Ganoderma lucidum (Lingzhi)/Placebo | HDL-C, TG, LDL-C/HDL-C, TC/HDL-C, SBP, DBP, WHR, BMI, FPG, Insulin, HOMA-IR, TC, LDL-C, Apo B, LDL-C/Apo B, FRAP, MDA, GPx dan SOD |
| Hu dan kawan-kawan ( 2014 ) | Hongkong | R, Komputer, DB | Dislipidemia | 40 (B) | 20/20 | 12 | Usia: 57,5 ± 8,4/54,7 ± 9,1
BMI: 25,9 ± 2,8/27,2 ± 4,7 |
3440 | Kapsul: Formula Multiherba Berbasis Crataegus (mengandung Ganoderma lucidum (Ling Zhi))/Placebo (pati dan pewarna makanan buatan) | Berat, TC, HDL-C, TG, LDL-C, Non-HDL-C, Glukosa puasa, HbA1c, Kreatinin, Protein total, Albumin, ALT & ALP |
| Klubp dkk. ( 2016 ) | Australia | R, Komputer, DB | T2DM dan Sindrom Metabolik | 84 (B) | 54/30 | 16 | Usia: 60,2 ± 10/57,1 ± 8,3
BMI: 34,1 ± 6,8/34,4 ± 7,4 |
3000 | Kapsul: Ganoderma lucidum dengan atau tanpa Cordyceps sinensis/Placebo (eksipien) | HbA1c, FPG, Tekanan arteri, TG, HDL-C, WC, BMI, CRP, TC, LDL-C, Apo A & Apo B |
| Chiu dan kawan-kawan ( 2017 ) | Indonesia | R, PC, DB, Silang | Sehat dengan disfungsi hati ringan | 42 (B) | Tanggal 21/21 | 24 | Usia: 40–54/40–54
BMI: 23,22 ± 2,93/23,26 ± 2,97 |
225 | Kapsul: Ganoderma lucidum /Placebo yang diperkaya triterpenoid dan peptida polisakarida (90% pati dan 10% residu GL) | Berat, BF, BMI, TEAC, TBARS, 8-OH-Dg, Thiol, GSH, SOD, CAT, G-6-PDH, GPx, GR, ALT & AST |
| Tsuk dkk. ( 2018 ) | Israel | R, Komputer, DB | Sehat | 96 (B) | 49/47 | 4 | Usia: 26,3 ± 3,21/26,3 ± 3,21
BMI: 23,53 ± 2,83/22,65 ± 2,30 |
tahun 1294 | Cairan oral dan kapsul: Cairan (mengandung Cordyceps sinensis + Ganoderma lucidum + shititake + rebung + madu + sorbet kalium + air murni dan kapsul (mengandung Ganoderma lucidum + Cordyceps sinensis + gel kedelai)/Placebo (sup jamur komersial dan kapsul glukosa))
Dengan cairan Cordyceps sinensis |
Berat Badan, Payudara, BMI, Tekanan Darah Siku, Tekanan Darah Tinggi dan Denyut Jantung |
| Gracián-Alcaide dkk. ( 2020 ) | Spanyol | R, Komputer, DB | Tua | 60 (B) | 30/30 | 14 | Usia: 85,9 ± 7,8/82,7 ± 9,2
BMI: 25,4 ± 3,8/26,1 ± 4,6 |
tahun 2000 | Sachet: Kombinasi elderberry ( Sambucus nigra L.) dan reishi ( Ganoderma lucidum )/Placebo (maltodekstrin) | Berat, Tekanan Darah Rendah (SBP) dan Tekanan Darah Rendah (DBP) |
| Rizal dkk. ( 2020 ) | Indonesia | R, komputer | Fibrilasi arteri | 38 (B) | tanggal 20/18 | 12 | Usia: 63,61 ± 8,50/62,50 ± 10,50
Indeks Massa Tubuh (IMT) : 26,30 ± 5,40/26,40 ± 4,00 |
750 | NR: Ganoderma lucidum polisakarida peptida/Placebo | BMI, SBP, DBP, SDM, NO, MDA, hs-CRP, IL-1b, IL-6 & TNF-α |
| Babamiri dan kawan-kawan ( 2022a ) | Bahasa Indonesia:Iran | R, Komputer, DB | Kegemukan | 69 (B) | 36/33 | 6 | Usia: 37,25/42,52 ± 10,62
BMI: 26,99 ± 1,02/26,84 ± 1,14 |
750 | Kapsul: Ganoderma lucidum /Placebo (tepung terigu) | Berat, BMI, WC, HC, WHR, MUAC, FBS, TC, LDL-C, HDL-C, TG, SBP & DBP |
| Sargowo dan kawan-kawan ( 2022 ) | Indonesia | Uji Coba Terpadu (RCT) | Kegemukan | 68 (NR) | 34/34 | 12 | Usia: 58,27 ± 2,5/59,5 ± 2,1
BMI: 31,02 ± 6,2/32,01 ± 7,1 |
540 | Kapsul: β-1,3/1,6-D-glukan dari ekstrak miselia ( Ganoderma lucidum )/Placebo | Kreatinin, NO, TNF-α, dan MDA |
| Chen dan kawan-kawan ( 2023 ) | Indonesia | R, Komputer, DB | Sehat | 135 (B) | 70/65 | 12 | Usia: 37,72 ± 7,36/39,11 ± 7,52
BMI: Tidak |
200 | Kapsul: Reishi β-glukan/Placebo (dekstrosa monohidrat) | AST, ALT & Kreatinin |
| Wardhani dkk. ( 2023 ) | Indonesia | R, DB, uji coba terkontrol | Sindrom kardiometabolik | 62 (NR) | Tanggal 31/31 | 8 | Usia: 58,27 ± 2,50/59,50 ± 2,10 BMI: 31,02 ± 6,20/32,01 ± 11,85 | 750 | Kapsul: GLPP Kering ( Ganoderma lucidum polysaccharide peptide)/Placebo | TNF-α, hs-CRP, MDA, SOD dan Kreatinin |
| Iser-Bem dan kawan-kawan ( 2024 ) | Brazil | komputer, basis data | Bebas dari penyakit neurodegeneratif | 39 (P) | Tanggal 23/16 | 8 | Usia: 68 ± 5,8/66,4 ± 5,9
BMI: 26,4 ± 5,5/26,5 ± 4,9 |
tahun 2000 | Kapsul: Ganoderma lucidum /Placebo (pati jagung) | Berat, BMI, BF, Massa ramping, WC, HC & WHR |
Singkatan: %BF, Persentase Lemak Tubuh; 8-OH-dG, 8-Hidroksiguanosin; ALP, Alkali Fosfatase; ALT, Alanin Aminotransferase; Apo A-1, Apolipoprotein AI; Apo B, Apolipoprotein B; AST, Aspartat Aminotransferase; B, Keduanya; BMI, Indeks Massa Tubuh; BUN, Nitrogen Urea Darah; CAT, Katalase; CRP, Protein C-reaktif; DB, Double Blind; DBP, Tekanan Darah Diastolik; ESR, Laju Sedimentasi Eritrosit; F, Wanita; FBS, Gula darah puasa; FPG, Glukosa Plasma Puasa; FRAP, Kemampuan mereduksi besi plasma; G-6-PDH, Glukosa-6-fosfat dehidrogenase; GLPP, Peptida Polisakarida Ganoderma lucidum ; GPx, Glutation Peroksidase; GR, Glutation reduktase; GSH, Total Glutathione; HbA1c, Hemoglobin A1c; HC, Lingkar Pinggul; HDL-C, Kolesterol Lipoprotein Densitas Tinggi; HOMA-IR, Penilaian Model Homeostatis untuk Resistensi Insulin; HR, Denyut Jantung; hs-CRP, Protein C-reaktif sensitivitas tinggi; HTN, Hipertensi; ICAM-1, Molekul adhesi antarsel-1; IFN-γ, Interferon-Gamma; IL-13, Interleukin-13; IL-18, Interleukin-18; IL-1b, Interleukin-1 Beta; IL-1ra, Antagonis reseptor interleukin-1; IL-3, Interleukin-3; IL-5, Interleukin-5; IL-6, Interleukin-6; IL-9, Interleukin-9; LDL-C, Kolesterol Lipoprotein Densitas Rendah; L, Pria; MDA, Malondialdehyde; MetS, Sindrom metabolik; MUAC, Lingkar lengan atas-tengah; NO, Nitric Oxide; NR, Tidak dilaporkan; PC, Terkontrol oleh Plasebo; R, Acak; RA, Artritis reumatoid; Ref, Referensi; SBP, Tekanan Darah Sistolik; SOD, Aktivitas Superoksida Dismutase; T2DM, Diabetes Melitus Tipe 2; TBARS, Zat Reaktif Asam Thiobarbiturat; TC, Kolesterol Total; TEAC, Kapasitas antioksidan setara Trolox; TG, Trigliserida; TNF-α, Tumor Necrosis Factor-alpha; VCAM-1, Molekul adhesi sel vaskular 1; WC, Lingkar Pinggang; WHR, Rasio Pinggang-Panggul.
Penelitian ini diterbitkan antara tahun 2004 dan 2024 dan dilakukan di berbagai negara, termasuk Australia (Klupp dkk. 2016 ), Brasil (Iser-Bem dkk. 2024 ), Tiongkok (Wachtel-Galor, Tomlinson, dkk. 2004 ; Wachtel-Galor, Szeto, dkk. 2004 ; Wen dkk. 2005 ), Hong Kong (Li et al. al. 2007 ; Chu et al. 2012 ; Hu et al. 2014 ), Iran (Babamiri et al. 2022a ), Israel (Tsuk et al. 2018 ) , Spanyol ( Gracián – Alcaide et al. 2020 ), Taiwan (Chiu et al. 2017 ; Chen et al. 2023 ), dan Amerika Serikat (Kelly-Pieper et al. 2009 ). Usia peserta dalam kelompok intervensi berkisar antara 26,3 hingga 85,9 tahun, dengan dosis Ganoderma bervariasi antara 200 hingga 11.200 mg/hari selama durasi intervensi 1–24 minggu. Ukuran sampel berkisar antara 10 hingga 135 peserta. Peserta datang dengan kondisi seperti asma alergi sedang hingga berat (Wen et al. 2005 ), asma RA (Li et al. 2007 ), asma (Kelly-Pieper et al. 2009 ), hipertensi dan/atau dislipidemia (Chu et al. 2012 ; Hu et al. 2014 ), T2DM dan sindrom metabolik (MetS) (Klupp et al. 2016 ), disfungsi hati ringan (Chiu et al. 2017 ), status lanjut usia (Gracián-Alcaide et al. 2020 ), AFib (Rizal et al. 2020 ), kelebihan berat badan (Babamiri et al. 2022a ), obesitas (Sargowo et al. 2022 ), CMS (Wardhani et al. 2023 ), tidak adanya penyakit neurodegeneratif (Iser-Bem et al. 2024 ) dan kesehatan umum atau kondisi non-spesifik (Wachtel-Galor, Tomlinson, dkk. 2004 ; Wachtel-Galor, Szeto, dkk. 2004 ; Tsuk dkk. 2018 ; Chen dkk. 2023 ).
Ukuran sampel untuk kelompok intervensi dan kontrol di berbagai hasil adalah sebagai berikut: BMI: n = 392 (intervensi: 216, kontrol: 176); BF: n = 178 (intervensi: 93, kontrol: 85); WC: n = 192 (intervensi: 113, kontrol: 79); berat: n = 347 (intervensi: 179, kontrol: 168); WHR: n = 131 (intervensi: 72, kontrol: 59); DBP: n = 287 (intervensi: 148, kontrol: 139); SBP: n = 287 (intervensi: 148, kontrol: 139); glukosa puasa: n = 236 (intervensi: 135, kontrol: 101); hs-CRP: n = 136 (intervensi: 69, kontrol: 67); TNF-α: n = 168 (intervensi: 85, kontrol: 83); HDL-C: n = 262 (intervensi: 146, kontrol: 116); LDL-C: n = 262 (intervensi: 146, kontrol: 116); TC: n = 262 (intervensi: 146, kontrol: 116); TG: n = 262 (intervensi: 146, kontrol: 116); ALT: n = 273 (intervensi: 141, kontrol: 132); AST: n = 233 (intervensi: 121, kontrol: 112); kreatinin: n = 361 (intervensi: 185, kontrol: 176); FRAP: n = 127 (intervensi: 64, kontrol: 63); GPx: n = 88 (intervensi: 44, kontrol: 44); MDA: n = 237 (intervensi: 121, kontrol: 116); SOD: n = 163 (intervensi: 83, kontrol: 80); HR: n = 135 (intervensi: 69, kontrol: 66).
3.3 Penilaian Data Kualitatif
Dengan menggunakan alat Penilaian Risiko Bias Cochrane, tidak ada penelitian yang dinilai berkualitas baik, satu penelitian dinilai cukup (Hu dkk. 2014 ), dan penelitian lainnya diklasifikasikan sebagai buruk (Klupp dkk. 2016 ; Iser-Bem dkk. 2024 ; Wachtel-Galor, Tomlinson, dkk. 2004 ; Wachtel-Galor, Szeto, dkk. 2004 ; Wen et al. 2005 ; Li et al. 2007 ; Chu et al. 2012 ; Rizal et al. 2020 ; Sargowo et al. 2022 ; Wardhani et al. 2023 ; Babamiri et al. 2022a ; Tsuk et al. 2018 ; Gracián-Alcaide et al. 2020 ; 2017 ; Chen dkk. 2023 ; Kelly-Pieper dkk. 2009 ) (Tabel 2 ).
| Studi, tahun (Ref.) | Pembuatan urutan acak | Penyembunyian alokasi | Pembutaan peserta & personel | Kebutaan penilaian hasil | Data hasil tidak lengkap | Pelaporan hasil selektif | Sumber bias lainnya | Kualitas keseluruhan |
|---|---|---|---|---|---|---|---|---|
| Wachtel-Galor, Tomlinson, dkk. ( 2004 ) | H | H | kamu | H | Saya | Saya | Saya | Miskin |
| Wachtel-Galor, Tomlinson, dkk. ( 2004 ) | H | H | Saya | H | H | Saya | Saya | Miskin |
| Wen dkk. ( 2005 ) | kamu | H | Saya | H | Saya | Saya | Saya | Miskin |
| Li dan kawan-kawan ( 2007 ) | Saya | Saya | Saya | H | H | Saya | Saya | Miskin |
| Kelly-Pieper dan kawan-kawan ( 2009 ) | kamu | H | Saya | H | Saya | Saya | Saya | Miskin |
| Chu dan kawan-kawan ( 2012 ) | kamu | H | kamu | H | H | Saya | Saya | Miskin |
| Hu dan kawan-kawan ( 2014 ) | Saya | H | Saya | Saya | Saya | Saya | Saya | Adil |
| Klubp dkk. ( 2016 ) | Saya | H | Saya | Saya | H | Saya | Saya | Miskin |
| Chiu dan kawan-kawan ( 2017 ) | kamu | H | Saya | H | Saya | Saya | Saya | Miskin |
| Tsuk dkk. ( 2018 ) | kamu | H | H | H | Saya | Saya | Saya | Miskin |
| Gracián-Alcaide dkk. ( 2020 ) | kamu | H | Saya | H | H | Saya | Saya | Miskin |
| Rizal dkk. ( 2020 ) | Saya | H | H | H | kamu | Saya | Saya | Miskin |
| Babamiri dan kawan-kawan ( 2022a ) | kamu | H | kamu | H | Saya | Saya | Saya | Miskin |
| Sargowo dan kawan-kawan ( 2022 ) | Saya | H | H | H | Saya | Saya | Saya | Miskin |
| Chen dan kawan-kawan ( 2023 ) | Saya | H | kamu | H | H | Saya | Saya | Miskin |
| Wardhani dkk. ( 2023 ) | kamu | H | kamu | H | kamu | Saya | Saya | Miskin |
| Iser-Bem dan kawan-kawan ( 2024 ) | H | H | kamu | H | H | Saya | Saya | Miskin |
Singkatan: H, risiko bias tinggi; L, risiko bias rendah; U, risiko bias tidak jelas.
3.4 Pengaruh Suplementasi Ganoderma terhadap Indeks Antropometri
Suplemen Ganoderma menunjukkan efek signifikan pada BMI (WMD = −0,43, 95% CI: −0,77 hingga −0,10; p = 0,011; I 2 = 40,8%, p = 0,106) (Gambar S1 ). Namun, suplementasi Ganoderma tidak menunjukkan efek signifikan terhadap BF (WMD = -0,42, 95% CI: -1,55 hingga 0,71; p = 0,467; I 2 = 0,0%, p = 0,647), WC (WMD = -0,45, 95% CI: -1,02 hingga 0,12; p = 0,123; I 2 = 0,0%, p = 0,753), berat (WMD = -0,15, 95% CI: -1,85 hingga 1,55; p = 0,865; I 2 = 0,0%, p = 0,725), atau WHR (WMD = 0,00, 95% CI: -0,01 hingga 0,01; p = 0,582; I2 = 18,5 %, p = 0,293).
Analisis sensitivitas menunjukkan bahwa pengecualian studi oleh Babamiri et al. (Babamiri et al. 2022a ) (WMD: -0,41, 95% CI: -0,86, 0,29) memengaruhi BMI secara signifikan. Uji Egger tidak menunjukkan bias publikasi yang signifikan untuk BMI ( p = 0,774), BF ( p = 0,202), WC ( p = 0,179), berat badan ( p = 0,678), dan WHR ( p = 0,500).
3.5 Efek Suplementasi Ganoderma terhadap Tekanan Darah
Suplementasi Ganoderma tidak menunjukkan efek signifikan terhadap DBP (WMD = -0,72, 95% CI: -3,43 hingga 1,99; p = 0,601; I 2 = 74,0%, p = 0,002) (Gambar S2 ) dan SBP (WMD = -1,50, 95% CI: -4,25 hingga 1,26; p = 0,286; I 2 = 52,4%, p = 0,062).
Analisis sensitivitas menunjukkan hasil yang konsisten bahkan setelah mengecualikan studi individual. Uji Egger menunjukkan tidak ada bias publikasi yang signifikan untuk DBP ( p = 0,757) atau SBP ( p = 0,483).
3.6 Efek Suplementasi Ganoderma terhadap Profil Glikemik
Meta-analisis kami tidak menunjukkan perubahan signifikan pada glukosa puasa (WMD = -0,03, 95% CI: -0,13 hingga 0,07; p = 0,555; I 2 = 0,0%, p = 0,952) (Gambar S3 ).
Analisis sensitivitas tidak menunjukkan perubahan pada parameter kelompok ini, dan juga tidak ada bias publikasi yang signifikan untuk glukosa puasa ( p = 0,785) berdasarkan uji Egger.
3.7 Efek Suplementasi Ganoderma terhadap Penanda Inflamasi
Suplementasi Ganoderma tidak menunjukkan efek signifikan pada hs-CRP (WMD = -0,28, 95% CI: -0,91 hingga 0,35; p = 0,388; I 2 = 91,9%, p < 0,001) (Gambar S4 ), dan TNF-α (WMD = -7,70, 95% CI: -27,84 hingga 12,43; p = 0,453; I 2 = 89,9%, p < 0,001).
Analisis sensitivitas menunjukkan stabilitas dalam parameter kelompok ini. Uji Egger menunjukkan tidak ada bias publikasi yang signifikan untuk TNF-α ( p = 0,725) atau hs-CRP ( p = 0,682).
3.8 Efek Suplementasi Ganoderma terhadap Profil Lipid
Temuan dari analisis kami menunjukkan bahwa suplementasi Ganoderma tidak menghasilkan manfaat signifikan pada HDL-C (WMD = 0,02, 95% CI: -0,04 hingga 0,08; p = 0,467; I 2 = 0,0%, p = 0,480) (Gambar S5 ), LDL-C (WMD = -0,13, 95% CI: -0,34 hingga 0,08; p = 0,225; I 2 = 54,9%, p = 0,050), TC (WMD = -0,18, 95% CI: -0,39 hingga 0,02; p = 0,083; I 2 = 32,8%, p = 0,190), dan TG (WMD = -0,12, 95% CI: -0,30 hingga 0,06; p = 0,197; I 2 = 61,2%, p = 0,024).
Analisis sensitivitas mengungkap bahwa pengecualian studi oleh Klupp et al. ( 2016 ) menghasilkan perubahan penting dalam hasil keseluruhan terkait kadar TC (WMD: -0,27, 95% CI: -0,44 hingga -0,10). Selain itu, penghapusan studi oleh Hu et al. ( 2014 ) mengubah efek keseluruhan pada TG (WMD: -0,16, 95% CI: -0,31 hingga -0,01). Lebih jauh, uji Egger tidak memberikan bukti bias publikasi dalam parameter profil lipid.
3.9 Efek Suplementasi Ganoderma terhadap Fungsi Hati
Suplementasi Ganoderma menunjukkan efek signifikan pada kreatinin (WMD = -0,14, 95% CI: -0,27 hingga -0,02; p = 0,028; I 2 = 80,0%, p < 0,001) (Gambar S6 ). Namun, suplementasi Ganoderma tidak menunjukkan efek signifikan pada ALT (WMD = -2,06, 95% CI: -7,64 hingga 3,52; p = 0,470: I 2 = 95,1%, p < 0,001) dan AST (WMD = -1,52, 95% CI: -5,09 hingga 2,04; p = 0,402: I 2 = 85,6%, p < 0,001).
Berbeda dengan parameter lain dalam kategori ini, analisis sensitivitas menunjukkan bahwa penghapusan studi oleh Wardhani et al. ( 2023 ) (WMD: -0,09, 95% CI: -0,22 hingga 0,30), Chen et al. (Chen et al. 2023 ) (WMD: -0,17, 95% CI: -0,39 hingga 0,05), dan Sargowo et al. (Sargowo et al. 2022 ) (WMD: -0,09, 95% CI: -0,20 hingga 0,03) memengaruhi hasil keseluruhan terkait kreatinin. Uji Egger tidak mengungkapkan bias publikasi signifikan untuk ALT ( p = 0,912) dan AST ( p = 0,671).
3.10 Efek Suplementasi Ganoderma terhadap Parameter Stres Oksidatif
Uji coba menunjukkan efek signifikan pada GPx (WMD = 2,29, 95% CI: 1,67–2,92; p < 0,001; I 2 = 0,0%, p = 0,986) (Gambar S7 ). Namun, tidak ada perubahan signifikan yang diamati dalam FRAP (WMD = -8,60, 95% CI: -72,07 hingga 54,87; p = 0,791; I 2 = 47,7%, p = 0,125), MDA (WMD = -0,07, 95% CI: -0,14 hingga 0,01; p = 0,071; I 2 = 96,0%, p < 0,001), atau SOD (WMD = 76,86, 95% CI: -21,51 hingga 175,23; p = 0,126; I 2 = 94,3%, p < 0,001).
Analisis sensitivitas mengungkapkan bahwa pengecualian studi oleh Chiu et al. ( 2017 ) mengubah hasil untuk GPx (WMD = 2,40, 95% CI: −0,80 hingga 5,61). Pengecualian studi oleh Wachtel-Galor, Tomlinson, et al. ( 2004 ) (WMD = −0,10, 95% CI: −0,19 hingga −0,01) dan Wachtel-Galor, Szeto, et al. ( 2004 ) (WMD = −0,09, 95% CI: −0,17 hingga −0,01) memengaruhi hasil keseluruhan untuk MDA. Studi oleh Chiu et al. ( 2017 ) juga memengaruhi analisis sensitivitas untuk SOD (WMD = 10,67, 95% CI: 5,61 hingga 15,72). Tidak terdeteksi bias publikasi untuk parameter stres oksidatif.
3.11 Efek Suplementasi Ganoderma terhadap Denyut Jantung
Hasil gabungan dari penelitian yang menyelidiki efek Ganoderma pada HR menunjukkan penurunan yang signifikan (WMD = −3,92, 95% CI: −7,45 hingga −0,40; p = 0,029; I 2 = 53,5%, p = 0,116) (Gambar S8 ).
Analisis sensitivitas menunjukkan bahwa pengecualian studi oleh Tsuk et al. ( 2018 ) (WMD = −2,07, 95% CI: −9,73 hingga 1,04) dan Rizal et al. (Rizal et al. 2020 ) (WMD = −4,34, 95% CI: −4,93 hingga 0,79) mengubah hasil gabungan untuk HR. Tidak ada bias publikasi yang terdeteksi untuk HR, sebagaimana dikonfirmasi oleh uji Egger.
3.12 Analisis Subkelompok
Analisis subkelompok berdasarkan kondisi kesehatan (penyakit kronis vs. individu yang berisiko tetapi umumnya sehat vs. populasi sehat), dosis Ganoderma (< 1400 mg/hari vs. ≥ 1400 mg/hari), durasi intervensi (≤ 8 minggu vs. > 8 minggu), usia peserta (< 50 tahun vs. ≥ 50 tahun), wilayah geografis (Asia Timur vs. Timur Tengah vs. Amerika, Oseania, dan Eropa), ukuran sampel (< 40 peserta vs. ≥ 40 peserta), dan tahun publikasi (≤ 2019 vs. > 2019) dirangkum dalam Tabel 3 .
| Studi N | Peserta N | Senjata pemusnah massal (95% CI) | P | Heterogenitas | ||||
|---|---|---|---|---|---|---|---|---|
| p heterogenitas | saya 2 | saya 2 | p antara subgrup | |||||
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap BMI | ||||||||
| Efek keseluruhan | 8 | 392 | -0,43 (-0,77, -0,10) | 0,011 | 0.106 | 40,8% | 0,077 tahun | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 145 | -0,13 (-0,43, 0,17) | 0.405 | 0.760 | 0,0% | Bahasa Indonesia | 0,009 |
| Individu yang berisiko tetapi umumnya sehat | 2 | 111 | -0,51 (-0,84, -0,18) | 0,003 | 0.418 | 0,0% | Bahasa Indonesia | |
| Sehat | 3 | 136 | -1,19 (-1,83, -0,55) | < 0,001 | 0,546 tahun | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 5 | 246 | -0,58 (-1,07, -0,09) | 0,020 | 0,051 tahun | 57,6% dari | Bahasa Indonesia | 0.197 |
| 1400 ≤ | 3 | 146 | -0,19 (-0,53, 0,16) | 0.297 | 0,925 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 4 | 187 | -0,82 (-1,30, -0,34) | 0,001 | 0.241 | 28,5% | Bahasa Indonesia | 0,015 |
| 8 < | 4 | 205 | -0,12 (-0,41, 0,17) | 0.410 | 0.904 | 0,0% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 4 | 184 | -0,77 (-1,28, -0,27) | 0,003 | 0.171 | 40,1% | Bahasa Indonesia | 0,032 |
| 50 ≤ | 4 | 208 | -0,13 (-0,43, 0,17) | 0.402 | 0,908 | 0,0% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 3 | 103 | -0,13 (-0,42, 0,17) | 0,389 | 0.792 | 0,0% | Bahasa Indonesia | 0,057 tahun |
| Timur Tengah | 3 | 166 | -0,91 (-1,48, -0,33) | 0,002 | 0,145 | 48,3% | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 2 | 123 | 0,05 (−1,38, 1,49) | 0.942 | 0.837 | 0,0% | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 3 | 100 | -0,14 (-0,44, 0,17) | 0.380 | 0.801 | 0,0% | Bahasa Indonesia | 0,041 tahun |
| 40 ≤ | 5 | 292 | -0,71 (-1,18, -0,25) | 0,003 | 0.222 | 30,0% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 5 | 246 | -0,60 (-1,21, 0,02) | 0,058 | 0,064 tahun | 54,9% | Bahasa Indonesia | 0.476 |
| Tahun 2019 < | 3 | 146 | -0,32 (-0,76, 0,11) | 0,147 tahun | 0.228 | 32,3% | Bahasa Indonesia | 0.476 |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap BF | ||||||||
| Efek keseluruhan | 4 | 178 | -0,42 (-1,55, 0,71) | 0.467 | 0.647 | 0,0% | 0.000 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma pada WC | ||||||||
| Efek keseluruhan | 3 | 192 | -0,45 (-1,02, 0,12) | 0.123 | 0.753 | 0,0% | 0.000 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap berat badan | ||||||||
| Efek keseluruhan | 7 | 347 | -0,15 (-1,85, 1,55) | 0,865 | 0,725 | 0,0% | 0.000 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 1 | 40 | 3,00 (−3,21, 9,21) | 0.344 | — | — | Bahasa Indonesia | 0,560 |
| Individu yang berisiko tetapi umumnya sehat | 3 | 171 | -0,66 (-3,09, 1,78) | 0,596 tahun | 0,348 tahun | 5,2% dari total | Bahasa Indonesia | |
| Sehat | 3 | 136 | -0,09 (-2,74, 2,56) | 0,948 tahun | 0.833 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 4 | 208 | -0,56 (-2,68, 1,56) | 0.607 | 0,559 | 0,0% | Bahasa Indonesia | 0,529 |
| 1400 ≤ | 3 | 139 | 0,58 (−2,25, 3,42) | 0,687 tahun | 0,555 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 4 | 205 | -0,97 (-3,22, 1,28) | 0.396 | 0,591 tahun | 0,0% | Bahasa Indonesia | 0.273 |
| 8 < | 3 | 142 | 0,95 (−1,64, 3,54) | 0.474 | 0,768 tahun | 0,0% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 4 | 208 | -0,56 (-2,68, 1,56) | 0.607 | 0,559 | 0,0% | Bahasa Indonesia | 0,529 |
| 50 ≤ | 3 | 139 | 0,58 (−2,25, 3,42) | 0,687 tahun | 0,555 | 0,0% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 2 | 82 | 1,14 (−2,33, 4,61) | 0,518 | 0.480 | 0,0% | Bahasa Indonesia | 0.654 |
| Timur Tengah | 3 | 166 | -0,85 (-3,31, 1,61) | 0.498 | 0.396 | 0,0% | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 2 | 99 | -0,06 (-3,24, 3,14) | 0,973 tahun | 0,507 tahun | 0,0% | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 1 | 39 | -1,60 (-7,17, 3,97) | 0,573 tahun | — | — | Bahasa Indonesia | 0,591 tahun |
| 40 ≤ | 6 | 308 | 0,00 (−1,78, 1,78) | 0,999 | 0.646 | 0,0% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 4 | 179 | 0,69 (−1,58, 2,96) | 0,551 tahun | 0.893 | 0,0% | Bahasa Indonesia | 0,276 tahun |
| Tahun 2019 < | 3 | 168 | -1,21 (-3,76, 1,35) | 0.354 | 0,398 | 0,0% | Bahasa Indonesia | 0,276 tahun |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap WHR | ||||||||
| Efek keseluruhan | 3 | 131 | 0,00 (−0,00, 0,01) | 0,582 | 0.293 | 18,5% | 0.000 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap DBP | ||||||||
| Efek keseluruhan | 6 | 287 | -0,72 (-3,43, 1,99) | 0.601 | 0,002 | 74,0% bahasa inggris | 8.003 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 2 | 61 | 0,67 (−8,34, 9,67) | 0.884 | 0,025 | 80,0% | Bahasa Indonesia | 0,695 tahun |
| Individu yang berisiko tetapi umumnya sehat | 2 | 129 | -2,59 (-7,71, 2,54) | 0.323 | 0,020 | 81,7% | Bahasa Indonesia | |
| Sehat | 2 | 97 | -0,23 (-2,85, 2,38) | 0.861 | 0.169 | 47,2% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 4 | 204 | -0,30 (-1,96, 1,36) | 0,725 | 0,345 tahun | 9,7% dari total | Bahasa Indonesia | 0,996 tahun |
| 1400 ≤ | 2 | 83 | -0,28 (-10,07, 9,52) | 0,956 | < 0,001 | 93,5% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 166 | -0,02 (-1,60, 1,56) | 0,977 tahun | 0,388 | 0,0% | Bahasa Indonesia | 0.698 |
| 8 < | 3 | 121 | -1,48 (-8,64, 5,67) | 0.686 | < 0,001 | 87,5% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 166 | -0,02 (-1,60, 1,56) | 0,977 tahun | 0,388 | 0,0% | Bahasa Indonesia | 0.698 |
| 50 ≤ | 3 | 121 | -1,48 (-8,64, 5,69) | 0.686 | < 0,001 | 87,5% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 2 | 61 | 0,67 (−8,34, 9,67) | 0.884 | 0,025 | 80,0% | Bahasa Indonesia | 0,013 |
| Timur Tengah | 3 | 166 | -0,02 (-1,60, 1,56) | 0,977 tahun | 0,388 | 0,0% | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 60 | -5,20 (-8,30, -2,10) | 0,001 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 2 | 61 | 0,67 (−8,34, 9,67) | 0.884 | 0,025 | 80,0% | Bahasa Indonesia | 0.664 |
| 40 ≤ | 4 | 226 | -1,42 (-4,09, 1,26) | 0.299 | 0,015 | 71,1% dari | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 3 | 120 | 1,10 (−2,12, 4,32) | 0,504 tahun | 0,035 | 70,1% dari | Bahasa Indonesia | 0.117 |
| Tahun 2019 < | 3 | 167 | -2,95 (-6,85, 0,95) | 0,139 | 0,058 | 64,9% | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap SBP | ||||||||
| Efek keseluruhan | 6 | 287 | -1,50 (-4,25, 1,26) | 0.286 | 0,062 | 52,4% dari | 5.748 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 2 | 61 | -4,00 (-18,67, 10,67) | 0,593 | 0,019 | 81,8% | Bahasa Indonesia | 0,797 tahun |
| Individu yang berisiko tetapi umumnya sehat | 2 | 129 | -2,19 (-7,71, 3,34) | 0.438 | 0,034 tahun | 77,8% dari total | Bahasa Indonesia | |
| Sehat | 2 | 97 | -0,53 (-3,20, 2,15) | 0,699 tahun | 0,944 tahun | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 4 | 204 | -0,95 (-3,83, 1,93) | 0.519 | 0.166 | 40,9% | Bahasa Indonesia | 0,878 |
| 1400 ≤ | 2 | 83 | -1,60 (-9,47, 6,26) | 0.690 | 0,050 | 74,0% bahasa inggris | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 166 | -0,12 (-2,22, 1,98) | 0.912 | 0.887 | 0,0% | Bahasa Indonesia | 0.291 |
| 8 < | 3 | 121 | -4,06 (-11,07, 2,95) | 0.256 | 0,042 tahun | 68,5% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 166 | -0,12 (-2,22, 1,98) | 0.912 | 0.887 | 0,0% | Bahasa Indonesia | 0.291 |
| 50 ≤ | 3 | 121 | -4,06 (-11,07, 2,95) | 0.256 | 0,042 tahun | 68,5% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 2 | 61 | -4,00 (-18,67, 10,67) | 0,593 | 0,019 | 81,8% | Bahasa Indonesia | 0,087 tahun |
| Timur Tengah | 3 | 166 | -0,12 (-2,22, 1,98) | 0.912 | 0.887 | 0,0% | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 60 | -5,10 (-9,06, -1,14) | 0,012 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 2 | 61 | -4,00 (-18,67, 10,67) | 0,593 | 0,019 | 81,8% | Bahasa Indonesia | 0.721 |
| 40 ≤ | 4 | 226 | -1,29 (-3,71, 1,12) | 0.294 | 0.173 | 39,9% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 3 | 120 | -0,09 (-2,59, 2,42) | 0,947 tahun | 0.656 | 0,0% | Bahasa Indonesia | 0.216 |
| Tahun 2019 < | 3 | 167 | -4,06 (-9,83, 1,71) | 0,168 | 0,019 | 74,9% | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap glukosa puasa | ||||||||
| Efek keseluruhan | 5 | 236 | -0,03 (-0,13, 0,07) | 0,555 | 0,952 | 0,0% | 0.000 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 4 | 167 | -0,03 (-0,24, 0,19) | 0.801 | 0,874 tahun | 0,0% | Bahasa Indonesia | 0,984 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 69 | -0,03 (-0,14, 0,08) | 0,594 tahun | — | — | Bahasa Indonesia | |
| Sehat | — | — | — | — | — | — | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 2 | 89 | -0,02 (-0,13, 0,09) | 0,687 tahun | 0,565 tahun | 0,0% | Bahasa Indonesia | 0,725 |
| 1400 ≤ | 3 | 147 | -0,07 (-0,32, 0,18) | 0,578 | 0.886 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 2 | 89 | -0,02 (-0,13, 0,09) | 0,687 tahun | 0,565 tahun | 0,0% | Bahasa Indonesia | 0,725 |
| 8 < | 3 | 147 | -0,07 (-0,32, 0,18) | 0,578 | 0.886 | 0,0% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 2 | 89 | -0,02 (-0,13, 0,09) | 0,687 tahun | 0,565 tahun | 0,0% | Bahasa Indonesia | 0,725 |
| 50 ≤ | 3 | 147 | -0,07 (-0,32, 0,18) | 0,578 | 0.886 | 0,0% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 2 | 63 | -0,07 (-0,33, 0,19) | 0,591 tahun | 0.623 | 0,0% | Bahasa Indonesia | 0,845 |
| Timur Tengah | 1 | 69 | -0,03 (-0,14, 0,08) | 0,594 tahun | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 2 | 104 | 0,06 (−0,31, 0,44) | 0.740 | 0.728 | 0,0% | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 2 | 43 | -0,01 (-0,24, 0,23) | 0,959 | 0,564 tahun | 0,0% | Bahasa Indonesia | 0.827 |
| 40 ≤ | 3 | 193 | -0,04 (-0,14, 0,07) | 0.531 | 0.853 | 0,0% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 4 | 167 | -0,03 (-0,24, 0,19) | 0.801 | 0,874 tahun | 0,0% | Bahasa Indonesia | 0,984 |
| Tahun 2019 < | 1 | 69 | -0,03 (-0,14, 0,08) | 0,594 tahun | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma pada hs-CRP | ||||||||
| Efek keseluruhan | 3 | 136 | -0,28 (-0,91, 0,35) | 0,388 | < 0,001 | 91,9% | 0,279 tahun | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap TNF-alpha | ||||||||
| Efek keseluruhan | 3 | 168 | -7,70 (-27,84, 12,43) | 0.453 | < 0,001 | 89,9% | ||
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap HDL-C | ||||||||
| Efek keseluruhan | 6 | 262 | 0,02 (−0,04, 0,08) | 0.467 | 0.480 | 0,0% | 0.000 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 147 | 0,02 (−0,08, 0,11) | 0.723 | 0.191 | 39,5% dari | Bahasa Indonesia | 0.611 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 69 | 0,08 (−0,05, 0,21) | 0.234 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 46 | -0,01 (-0,14, 0,12) | 0.882 | 0.704 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 2 | 79 | 0,06 (−0,05, 0,17) | 0.271 | 0.622 | 0,0% | Bahasa Indonesia | 0.414 |
| 1400 ≤ | 4 | 183 | 0,01 (−0,06, 0,08) | 0.842 | 0.317 | 15,0% dari | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 115 | 0,033 (−0,06, 0,13) | 0.472 | 0,586 tahun | 0,0% | Bahasa Indonesia | 0.805 |
| 8 < | 3 | 147 | 0,02 (−0,08, 0,11) | 0.723 | 0.191 | 39,5% dari | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 115 | 0,03 (−0,06, 0,13) | 0.472 | 0,586 tahun | 0,0% | Bahasa Indonesia | 0.805 |
| 50 ≤ | 3 | 147 | 0,02 (−0,08, 0,11) | 0.723 | 0.191 | 39,5% dari | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 4 | 109 | 0,01 (−0,07, 0,10) | 0.753 | 0.321 | 14,2% | Bahasa Indonesia | 0.608 |
| Timur Tengah | 1 | 69 | 0,08 (−0,05, 0,21) | 0.234 | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 84 | 0,00 (−0,09, 0,09) | 1.000 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 3 | 69 | 0,05 (−0,05, 0,15) | 0,349 tahun | 0,360 | 2,2% | Bahasa Indonesia | 0.519 |
| 40 ≤ | 3 | 193 | 0,01 (−0,06, 0,08) | 0.819 | 0.363 | 1,2% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 5 | 69 | 0,01 (−0,05, 0,07) | 0.802 | 0.471 | 0,0% | Bahasa Indonesia | 0.329 |
| Tahun 2019 < | 1 | 193 | 0,08 (−0,05, 0,21) | 0.234 | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap LDL-C | ||||||||
| Efek keseluruhan | 6 | 262 | -0,13 (-0,34, 0,08) | 0,225 | 0,050 | 54,9% | 0,035 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 147 | 0,03 (−0,33, 0,28) | 0,869 | 0,146 tahun | 48,1% dari | Bahasa Indonesia | 0,145 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 69 | -0,03 (-0,19, 0,13) | 0.712 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 46 | -0,46 (-0,88, -0,05) | 0,027 | 0.236 | 28,8% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 2 | 79 | -0,05 (-0,20, 0,10) | 0,533 | 0.445 | 0,0% | Bahasa Indonesia | 0.522 |
| 1400 ≤ | 4 | 183 | -0,18 (-0,55, 0,19) | 0.341 | 0,017 tahun | 70,7% dari | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 115 | -0,27 (-0,66, 0,12) | 0.181 | 0,038 | 69,4% | Bahasa Indonesia | 0,339 |
| 8 < | 3 | 147 | -0,03 (-0,33, 0,28) | 0,869 | 0,146 tahun | 48,1% dari | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 115 | -0,27 (-0,66, 0,12) | 0.181 | 0,038 | 69,4% | Bahasa Indonesia | 0,339 |
| 50 ≤ | 3 | 147 | -0,03 (-0,33, 0,28) | 0,869 | 0,146 tahun | 48,1% dari | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 4 | 109 | -0,30 (-0,56, -0,05) | 0,018 | 0,285 | 20,8% | Bahasa Indonesia | 0,040 |
| Timur Tengah | 1 | 69 | -0,03 (-0,19, 0,13) | 0.712 | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 84 | 0,20 (−0,11, 0,51) | 0.203 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 3 | 69 | -0,31 (-0,68, 0,06) | 0,105 | 0.151 | 47,2% | Bahasa Indonesia | 0.194 |
| 40 ≤ | 3 | 193 | -0,02 (-0,24, 0,20) | 0.863 | 0.142 | 48,7% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 5 | 69 | -0,18 (-0,49, 0,12) | 0.231 | 0,033 | 61,8% | Bahasa Indonesia | 0,376 tahun |
| Tahun 2019 < | 1 | 193 | -0,03 (-0,19, 0,13) | 0.712 | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap TC | ||||||||
| Efek keseluruhan | 6 | 262 | -0,18 (-0,39, 0,02) | 0,083 tahun | 0.190 | 32,8% | 0,020 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 147 | 0,02 (−0,23, 0,26) | 0.899 | 0.397 | 0,0% | Bahasa Indonesia | 0,069 tahun |
| Individu yang berisiko tetapi umumnya sehat | 1 | 69 | -0,25 (-0,48, -0,02) | 0,033 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 46 | -0,50 (-0,90, -0,11) | 0,013 | 0.611 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 2 | 79 | -0,26 (-0,48, -0,04) | 0,020 | 0.791 | 0,0% | Bahasa Indonesia | 0,549 tahun |
| 1400 ≤ | 4 | 183 | -0,14 (-0,47, 0,19) | 0.403 | 0,092 | 53,5% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 115 | -0,31 (-0,51, -0,12) | 0,002 | 0.491 | 0,0% | Bahasa Indonesia | 0,041 tahun |
| 8 < | 3 | 147 | 0,02 (−0,23, 0,26) | 0.899 | 0.397 | 0,0% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 115 | -0,31 (-0,51, -0,12) | 0,002 | 0.491 | 0,0% | Bahasa Indonesia | 0,041 tahun |
| 50 ≤ | 3 | 147 | 0,02 (−0,23, 0,26) | 0.899 | 0.397 | 0,0% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 4 | 109 | -0,29, (-0,55, -0,04) | 0,025 | 0,545 tahun | 0,0% | Bahasa Indonesia | 0,071 tahun |
| Timur Tengah | 1 | 69 | -0,25 (-0,48, -0,02) | 0,033 | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 84 | 0,20 (−0,16, 0,56) | 0.281 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 3 | 69 | -0,37 (-0,69, -0,05) | 0,024 | 0.461 | 0,0% | Bahasa Indonesia | 0,199 |
| 40 ≤ | 3 | 193 | -0,09 (-0,37, 0,19) | 0,526 | 0.121 | 52,7% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 5 | 193 | -0,16 (-0,44, 0,12) | 0.263 | 0.143 | 41,7% | Bahasa Indonesia | 0.633 |
| Tahun 2019 < | 1 | 69 | -0,25 (-0,48, -0,02) | 0,033 | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap TG | ||||||||
| Efek keseluruhan | 6 | 262 | -0,12 (-0,30, 0,06) | 0.197 | 0,024 | 61,2% | 0,025 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 147 | 0,05 (−0,51, 0,61) | 0.861 | 0,024 | 73,2% | Bahasa Indonesia | 0,073 tahun |
| Individu yang berisiko tetapi umumnya sehat | 1 | 69 | -0,03 (-0,16, 0,10) | 0.639 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 46 | -0,24 (-0,39, -0,10) | 0,001 | 0,759 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 2 | 79 | -0,12 (-0,36, 0,11) | 0.304 | 0.103 | 62,5% | Bahasa Indonesia | 0.773 |
| 1400 ≤ | 4 | 183 | -0,06 (-0,40, 0,28) | 0.716 | 0,029 | 66,7% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 115 | -0,16 (-0,32, 0,01) | 0,060 | 0,083 tahun | 59,9% dari | Bahasa Indonesia | 0.489 |
| 8 < | 3 | 147 | 0,05 (−0,51, 0,61) | 0.861 | 0,024 | 73,2% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 115 | -0,16 (-0,32, 0,01) | 0,060 | 0,083 tahun | 59,9% dari | Bahasa Indonesia | 0.489 |
| 50 ≤ | 3 | 147 | 0,05 (−0,51, 0,61) | 0.861 | 0,024 | 73,2% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 4 | 109 | -0,18 (-0,44, 0,09) | 0.186 | 0,047 tahun | 62,3% | Bahasa Indonesia | 0.511 |
| Timur Tengah | 1 | 69 | -0,03 (-0,16, 0,10) | 0.639 | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 84 | 0,10 (−0,40, 0,60) | 0,695 tahun | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 3 | 69 | -0,26 (-0,40, -0,13) | < 0,001 | 0.691 | 0,0% | Bahasa Indonesia | 0,028 |
| 40 ≤ | 3 | 193 | 0,11 (−0,19, 0,42) | 0.467 | 0.142 | 48,7% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 5 | 69 | -0,14 (-0,38, 0,10) | 0.250 | 0,051 tahun | 57,6% dari | Bahasa Indonesia | 0.425 |
| Tahun 2019 < | 1 | 193 | -0,03 (-0,16, 0,10) | 0.639 | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap ALT | ||||||||
| Efek keseluruhan | 5 | 273 | -2,06 (-7,64, 3,52) | 0.470 | < 0,001 | 95,1% dari | 36.848 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 2 | 60 | 1,59 (−1,80, 4,97) | 0.358 | 0.817 | 0,0% | Bahasa Indonesia | 0.000 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 42 | -10,78 (-12,75, -8,81) | < 0,001 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 171 | -0,56 (-1,82, 0,71) | 0,389 | 0.754 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 3 | 197 | -3,25 (-11,18, 4,68) | 0.421 | < 0,001 | 97,4% | Bahasa Indonesia | 0.461 |
| 1400 ≤ | 2 | 76 | -0,02 (-3,39, 3,36) | 0,993 tahun | 0.468 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 2 | 56 | 0,34 (−3,10, 3,77) | 0.848 | 0.346 | 0,0% | Bahasa Indonesia | 0.380 |
| 8 < | 3 | 217 | -3,49 (-11,32, 4,34) | 0.382 | < 0,001 | 97,4% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 4 | 233 | -2,81 (-9,29, 3,67) | 0,395 | < 0,001 | 96,2% | Bahasa Indonesia | 0.326 |
| 50 ≤ | 1 | 40 | 1,20 (−3,50, 5,90) | 0.617 | — | — | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 4 | 253 | -2,99 (-9,40, 3,41) | 0,360 | < 0,001 | 96,1% | Bahasa Indonesia | 0.224 |
| Timur Tengah | — | — | — | — | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 20 | 2,00 (−2,87, 6,87) | 0.421 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 2 | 56 | 0,34 (3,10, 3,77) | 0.848 | 0.346 | 0,0% | Bahasa Indonesia | 0.380 |
| 40 ≤ | 3 | 217 | -3,49 (-11,32, 4,34) | 0.382 | < 0,001 | 97,4% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 4 | 138 | -2,41 (-9,86, 5,04) | 0,526 | < 0,001 | 93,2% | Bahasa Indonesia | 0.620 |
| Tahun 2019 < | 1 | 135 | -0,50 (-1,81, 0,81) | 0.454 | — | — | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Chlorella terhadap AST | ||||||||
| Efek keseluruhan | 4 | 233 | -1,52 (-5,09, 2,04) | 0.402 | < 0,001 | 85,6% | 10.540 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap Kreatinin | ||||||||
| Efek keseluruhan | 6 | 361 | -0,14 (-0,27, -0,02) | 0,028 | < 0,001 | 80,0% | 0,015 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 122 | -0,18 (-0,53, 0,17) | 0.318 | 0,005 | 81,2% | Bahasa Indonesia | 0,015 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 68 | -0,39 (-0,57, -0,21) | < 0,001 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 171 | -0,04 (-0,19, 0,12) | 0.644 | 0,030 | 78,7% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 4 | 285 | -0,19 (-0,34, -0,04) | 0,011 | < 0,001 | 85,1% dari | Bahasa Indonesia | 0,016 |
| 1400 ≤ | 2 | 76 | 0,06 (−0,08, 0,20) | 0.411 | 0,985 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 118 | -0,10 (-0,32, 0,13) | 0.410 | 0,001 | 85,6% | Bahasa Indonesia | 0.456 |
| 8 < | 3 | 243 | -0,23 (-0,50, 0,04) | 0,094 tahun | 0,009 | 78,8% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 3 | 191 | -0,03 (-0,13, 0,07) | 0,549 tahun | 0,028 | 72,1% dari | Bahasa Indonesia | 0.000 |
| 50 ≤ | 3 | 170 | -0,39 (-0,52, -0,25) | < 0,001 | 0,990 | 0,0% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 5 | 341 | -0,19 (-0,35, -0,02) | 0,029 | < 0,001 | 81,9% | Bahasa Indonesia | 0,075 hari |
| Timur Tengah | — | — | — | — | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | 1 | 20 | 0,00 (−0,12, 0,12) | 1.000 | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 2 | 56 | 0,02 (−0,07, 0,12) | 0.602 | 0,525 | 0,0% | Bahasa Indonesia | 0,015 |
| 40 ≤ | 4 | 305 | -0,27 (-0,50, -0,05) | 0,016 | 0,001 | 82,3% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 3 | 96 | 0,02 (−0,07, 0,12) | 0.602 | 0.817 | 0,0% | Bahasa Indonesia | 0,018 |
| Tahun 2019 < | 3 | 265 | -0,28 (-0,51, -0,05) | 0,019 | < 0,001 | 88,2% | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma pada FRAP | ||||||||
| Efek keseluruhan | 4 | 127 | -8,60 (-72,07, 54,87) | 0.791 | 0,125 | 47,7% dari | tahun 1900 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma pada GPx | ||||||||
| Efek keseluruhan | 3 | 88 | 2.29 (1.67, 2.92) | < 0,001 | 0,986 tahun | 0,0% | 0.000 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap MDA | ||||||||
| Efek keseluruhan | 6 | 237 | -0,07 (-0,14, 0,01) | 0,071 tahun | < 0,001 | 96,0% bahasa inggris | 0,005 | |
| Kondisi kesehatan | ||||||||
| Penyakit kronis | 3 | 123 | -0,18 (-0,38, 0,02) | 0,072 | 0,008 | 79,2% | Bahasa Indonesia | 0.000 |
| Individu yang berisiko tetapi umumnya sehat | 1 | 68 | -0,08 (-0,10, -0,06) | < 0,001 | — | — | Bahasa Indonesia | |
| Sehat | 2 | 46 | 0,02 (0,02, 0,02) | < 0,001 | 0.860 | 0,0% | Bahasa Indonesia | |
| Dosis Ganoderma | ||||||||
| tahun 1400 < | 4 | 178 | -0,10 (-0,19, -0,01) | 0,024 | < 0,001 | 97,6% | Bahasa Indonesia | 0,064 tahun |
| 1400 ≤ | 2 | 59 | 0,01 (−0,07, 0,09) | 0.782 | 0.630 | 0,0% | Bahasa Indonesia | |
| Durasi intervensi | ||||||||
| 8 ≥ | 3 | 108 | -0,06 (-0,20, 0,09) | 0.436 | < 0,001 | 88,5% | Bahasa Indonesia | 0.724 |
| 8 < | 3 | 129 | -0,09 (-0,19, 0,01) | 0,086 tahun | 0,079 tahun | 60,5% | Bahasa Indonesia | |
| Usia intervensi | ||||||||
| 50 > | 2 | 46 | 0,02 (0,02, 0,02) | < 0,001 | 0.860 | 0,0% | Bahasa Indonesia | 0,005 |
| 50 ≤ | 4 | 191 | -0,14 (-0,24, -0,03) | 0,015 | 0,008 | 74,7% | Bahasa Indonesia | |
| Wilayah geografis | ||||||||
| Asia Timur | 6 | 237 | -0,07 (-0,14, 0,01) | 0,071 tahun | < 0,001 | 96,0% bahasa inggris | Bahasa Indonesia | |
| Timur Tengah | — | — | — | — | — | — | Bahasa Indonesia | |
| Amerika, Oseania dan Eropa | — | — | — | — | — | — | Bahasa Indonesia | |
| Ukuran sampel | ||||||||
| 40 > | 4 | 107 | -0,01 (-0,09, 0,07) | 0,759 | 0,055 | 60,5% | Bahasa Indonesia | 0.132 |
| 40 ≤ | 2 | 130 | -0,15 (-0,32, 0,01) | 0,069 tahun | 0,009 | 85,2% | Bahasa Indonesia | |
| Tahun Terbit | ||||||||
| Tahun 2019 ≥ | 3 | 69 | 0,02 (0,02, 0,02) | < 0,001 | 0.871 | 0,0% | Bahasa Indonesia | 0,009 |
| Tahun 2019 < | 3 | 168 | -0,19 (-0,35, -0,03) | 0,017 tahun | 0,006 | 80,7% | Bahasa Indonesia | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap SOD | ||||||||
| Efek keseluruhan | 4 | 163 | 76,86 (−21,51, 175,23) | 0.126 | < 0,001 | 94,3% | 8000 | |
| Analisis dan hasil subkelompok suplementasi Ganoderma terhadap HR | ||||||||
| Efek keseluruhan | 3 | 135 | -3,92 (-7,45, -0,40) | 0,029 | 0.116 | 53,5% | 5.168 | |
Singkatan: ALP, alkaline phosphatase; ALT, alanine aminotransferase; AST, aspartate aminotransferase; BMI, body mass index; CI, confidence interval; DBP, diastolic blood pressure; FRAP, ferric reduction ability of plasma; GPx, glutathione peroxidase; HDL-C, high-density lipoprotein cholesterol; HR, Heart rate; hs-CRP, high-sensitivity C-reactive protein; IL-6, interleukin-6; INT, intervention group; LDL-C, low-density lipoprotein cholesterol; MDA, malondialdehyde; NA, tidak berlaku; SBP, systolic blood pressure; SOD, superoxide dismutase; TC, total cholesterol; TG, triglycerides; TNF-α, tumor necrosis factor-alpha; WC, waist circles; WHR, waist-to-hip ratio; WMD, weighted mean difference. Nilai yang dicetak tebal secara statistik signifikan.
Dalam analisis subkelompok kondisi kesehatan, suplementasi Ganoderma tidak menunjukkan efek signifikan pada pasien dengan penyakit kronis. Pada individu yang berisiko tetapi umumnya sehat, perubahan signifikan diamati pada kadar ALT dan kreatinin, sementara pada individu yang sehat, peningkatan dicatat pada kadar LDL-C dan TG. Suplementasi Ganoderma secara signifikan memengaruhi BMI, TC, dan MDA pada populasi yang berisiko dan sehat. Namun, tidak ditemukan efek substansial pada berat badan, DBP, SBP, glukosa puasa, atau HDL-C.
Dalam analisis subkelompok dosis, suplementasi Ganoderma pada dosis < 1400 mg/hari menghasilkan perbaikan signifikan pada BMI, TC, kreatinin, dan MDA. Sebaliknya, dosis ≥ 1400 mg/hari tidak menghasilkan perubahan signifikan. Mengenai durasi intervensi, suplementasi Ganoderma selama ≤ 8 minggu secara signifikan meningkatkan BMI dan TC, sedangkan intervensi yang berlangsung > 8 minggu tidak menunjukkan efek signifikan.
Analisis subkelompok usia menunjukkan bahwa suplementasi Ganoderma secara signifikan meningkatkan BMI dan TC pada peserta berusia < 50 tahun. Di antara mereka yang berusia ≥ 50 tahun, perubahan penting diamati pada kadar kreatinin. Selain itu, kadar MDA terpengaruh secara signifikan pada kedua kelompok usia. Tidak ada efek signifikan yang diamati untuk berat badan, DBP, SBP, glukosa puasa, HDL-C, LDL-C, TG, atau ALT di seluruh subkelompok usia.
Dalam analisis subkelompok geografis, suplementasi Ganoderma meningkatkan kadar LDL-C dan kreatinin pada peserta Asia Timur. Studi yang dilakukan di Timur Tengah menunjukkan efek signifikan pada BMI, sementara penelitian dari Amerika, Oseania, dan Eropa menunjukkan dampak signifikan pada DBP dan SBP. Kadar TC dipengaruhi pada kelompok Asia Timur dan Timur Tengah. Tidak ditemukan perubahan signifikan pada berat badan, glukosa puasa, HDL-C, TG, ALT, atau MDA pada kelompok geografis mana pun.
Untuk penelitian dengan < 40 partisipan, suplementasi Ganoderma secara signifikan meningkatkan kadar TC, TG, dan ALT. Sebaliknya, penelitian dengan ≥ 40 partisipan menunjukkan efek signifikan pada BMI dan kreatinin. Tidak ada efek signifikan yang diamati untuk berat badan, DBP, SBP, glukosa puasa, HDL-C, LDL-C, atau MDA di seluruh subkelompok ukuran sampel.
Analisis subkelompok berdasarkan tahun penerbitan menunjukkan adanya perbaikan signifikan pada kadar TC dan kreatinin dalam penelitian yang diterbitkan sebelum tahun 2019. Kadar MDA terpengaruh secara signifikan dalam penelitian yang dilakukan sebelum dan sesudah tahun 2019. Namun, tidak ada perubahan signifikan yang dicatat untuk BMI, berat badan, DBP, SBP, glukosa puasa, HDL-C, LDL-C, TG, atau ALT di kedua kelompok.
3.13 Penilaian KELAS
Profil GRADE untuk suplementasi Ganoderma, yang merangkum tingkat kepastian dalam hasil, disajikan dalam Tabel 4. Kualitas bukti dinilai sangat rendah di semua hasil.
| Hasil | Risiko bias | Ketidakkonsistenan | Ketidaklangsungan | Ketidaktepatan | bias publikasi | Nomor (INT/CON) | Senjata pemusnah massal (95% CI) | Kualitas bukti |
|---|---|---|---|---|---|---|---|---|
| Indeks Massa Tubuh (IMT) | Sangat serius | Tidak serius | Tidak serius | Serius b | Tidak ada | 216/176 | -0,43 (-0,77, -0,10) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Persentase lemak tubuh | Sangat serius | Tidak serius | Serius c | Sangat serius b | Tidak ada | 93/85 | -0,42 (-1,55, 0,71) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Toilet umum | Sangat serius | Tidak serius | Serius c | Sangat serius b,d , b,d | Tidak ada | 113/79 | -0,45 (-1,02, 0,12) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Berat | Serius a | Tidak serius | Tidak serius | Sangat serius b,d , b,d | Tidak ada | 179/168 | -0,15 (-1,85, 1,55) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| WHR | Sangat serius | Tidak serius | Serius c | Sangat serius b,d , b,d | Tidak ada | 72/59 | 0,00 (−0,00, 0,01) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| DBP | Sangat serius | Serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 148/139 | -0,72 (-3,43, 1,99) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| SBP | Sangat serius | Serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 148/139 | -1,50 (-4,25, 1,26) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Glukosa puasa | Serius a | Tidak serius | Serius c | Sangat serius b,d , b,d | Tidak ada | 135/101 | -0,03 (-0,13, 0,07) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| hs-CRP | Sangat serius | Sangat serius e | Sangat serius c | Sangat serius b,d , b,d | Tidak ada | 69/67 | -0,28 (-0,91, 0,35) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| TNF-α | Sangat serius | Sangat serius e | Sangat serius c | Sangat serius b,d , b,d | Tidak ada | 85/83 | -7,70 (-27,84, 12,43) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| HDL-C | Sangat serius | Tidak serius | Serius c | Sangat serius b,d , b,d | Tidak ada | 146/116 | 0,02 (−0,04, 0,08) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| LDL-C | Serius a | Serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 146/116 | -0,13 (-0,34, 0,08) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| TC | Serius a | Serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 146/116 | -0,18 (-0,39, 0,02) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Tg | Sangat serius | Serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 146/116 | -0,12 (-0,30, 0,06) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| ALT | Serius a | Sangat serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 141/132 | -2,06 (-7,64, 3,52) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Bahasa Inggris | Sangat serius | Sangat serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | nomor 121/112 | -1,52 (-5,09, 2,04) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| Kreatinin | Serius a | Sangat serius e | Serius c | Serius b | Tidak ada | 185/176 | -0,14 (-0,27, -0,02) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| FRAP | Sangat serius | Tidak serius | Serius c | Sangat serius b,d , b,d | Tidak ada | 64/63 | -8,60 (-72,07, 54,87) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| GPx | Sangat serius | Tidak serius | Serius c | Serius b | Tidak ada | 44/44 | 2.29 (1.67, 2.92) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| MDA | Sangat serius | Sangat serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | nomor 121/116 | -0,07 (-0,14, 0,01) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| MERUMPUT | Sangat serius | Sangat serius e | Serius c | Sangat serius b,d , b,d | Tidak ada | 83/80 | 76,86 (−21,51, 175,23) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
| SDM | Sangat serius | Serius e | Serius c | Serius b | Tidak ada | 69/66 | -3,92 (-7,45, -0,40) | Bahasa Indonesia: ⊕◯◯◯
Sangat rendah |
Singkatan: ALP, alkaline phosphatase; ALT, alanine aminotransferase; AST, aspartate aminotransferase; BMI, indeks massa tubuh; CI, interval kepercayaan; DBP, tekanan darah diastolik; FRAP, kemampuan reduksi besi plasma; GPx, glutathione peroksidase; HDL, lipoprotein densitas tinggi; HR, denyut jantung; hs-CRP, protein C-reaktif sensitivitas tinggi; IL-6, interleukin-6; INT, kelompok intervensi; LDL, lipoprotein densitas rendah; MDA, malondialdehyde; SBP, tekanan darah sistolik; SOD, superoksida dismutase; TC, kolesterol total; TG, trigliserida; TNF-α, faktor nekrosis tumor-alfa; WC, lingkar pinggang; WHR, rasio pinggang-panggul; WMD, perbedaan rata-rata tertimbang. a Diturunkan karena lebih dari 50% peserta berasal dari studi bias risiko tinggi. b Diturunkan karena peserta yang diikutsertakan kurang dari 400 orang. c Diturunkan peringkatnya karena sifatnya yang tidak langsung di negara tersebut. d Diturunkan karena 95% CI melewati ambang batas yang diinginkan. e Nilai I 2 > 50% (atau Heterogenitas antar penelitian tinggi).
4 Diskusi
4.1 Ringkasan Temuan
Dalam penelitian ini, data dari 17 RCT yang melibatkan 971 partisipan digabungkan dan dianalisis. Temuan menunjukkan bahwa suplementasi G. lucidum secara signifikan memengaruhi BMI (WMD = -0,43 kg/m 2 , 95% CI: -0,77 hingga -0,10, p = 0,011), kreatinin (WMD = -0,14 mg/dL, 95% CI: -0,27 hingga -0,02, p = 0,028), GPx (WMD = 2,29 U/g Hb, 95% CI: 1,67 hingga 2,92, p < 0,001), dan denyut jantung (WMD = -3,92 bpm, 95% CI: -7,45 hingga -0,40, p = 0,029). Namun, suplementasi G. lucidum tidak menunjukkan efek signifikan pada BF, WC, WHR, DBP, SBP, glukosa puasa, hs-CRP, TNF-α, HDL-C, LDL-C, TC, TG, ALT, AST, FRAP, MDA, atau SOD. Meta-analisis dari 17 RCT ini menemukan efek sederhana suplementasi Ganoderma lucidum pada BMI, kreatinin, GPx, dan HR, tetapi tidak ada dampak signifikan pada BP, profil lipid, atau penanda inflamasi.
Sejauh pengetahuan kami, tinjauan sistematis dan meta-analisis dosis-respons ini adalah yang pertama menggunakan metodologi GRADE untuk menyelidiki efek suplementasi Ganoderma pada hasil kardiometabolik pada orang dewasa. Kurangnya efek signifikan pada faktor risiko kardiovaskular utama seperti tekanan darah, profil lipid, dan penanda inflamasi (hs-CRP, TNF-α) memerlukan penjelasan lebih lanjut. Beberapa faktor dapat menjelaskan temuan nihil ini. Pertama, senyawa bioaktif dalam G. lucidum , seperti polisakarida dan triterpen, mungkin memiliki potensi atau bioavailabilitas terbatas pada manusia dibandingkan dengan model praklinis, berpotensi tidak cukup untuk menghasilkan perubahan yang terdeteksi pada tekanan darah, lipid, atau inflamasi dalam durasi uji coba dan dosis yang dipelajari (berkisar dari 225 hingga 11.200 mg/hari). Misalnya, triterpen, yang dihipotesiskan menghambat ACE dan mengurangi stres oksidatif, mungkin memerlukan konsentrasi yang lebih tinggi atau paparan yang lebih lama untuk memengaruhi tekanan darah secara signifikan, seperti yang disarankan oleh penelitian pada hewan (Shevelev et al. 2018 ). Demikian pula, efek antiinflamasi polisakarida (misalnya, melalui modulasi sitokin) yang diamati secara in vitro mungkin tidak diterjemahkan secara efektif ke penanda inflamasi sistemik manusia seperti hs-CRP atau TNF-α karena perbedaan metabolisme atau interaksi mikrobiota usus (Chang et al. 2015 ). Kedua, heterogenitas yang nyata dalam protokol intervensi—mencakup dosis, formulasi (misalnya, ekstrak, spora), dan durasi (1–24 minggu)—kemungkinan mengencerkan efek potensial, seperti yang tercermin dalam nilai I 2 sedang hingga tinggi untuk BP ( I 2 = 74,0% untuk DBP, 52,4% untuk SBP) dan inflamasi ( I 2 = 91,9% untuk hs-CRP, 89,9% untuk TNF-α). Ketiga, ukuran sampel yang kecil (sebagian besar penelitian < 100 peserta) dan kelemahan metodologis dari RCT yang disertakan, yang dinilai dominan sebagai kualitas ‘Buruk’ dengan bukti GRADE yang sangat rendah, mungkin tidak memiliki kekuatan statistik untuk mendeteksi perubahan yang halus tetapi bermakna dalam hasil ini. Akhirnya, karakteristik dasar peserta, yang sering kali mencakup individu yang sehat atau berisiko dengan profil BP, lipid, atau inflamasi yang normal, mungkin telah membatasi ruang lingkup untuk perbaikan, efek batas atas yang tidak diamati dalam model praklinis dengan patologi yang diinduksi (misalnya, HTN, dislipidemia). Pengurangan BMI yang diamati (-0,43 kg/m 2 ) secara statistik signifikan tetapi berada di bawah ambang batas yang bermakna secara klinis ≥ 0,5–1 kg/m 2 untuk mengurangi risiko kardiometabolik (Donnelly et al. 2009 ). Demikian pula, pengurangan HR (-3,92 bpm) mungkin memiliki dampak klinis yang terbatas pada populasi normotensi tetapi dapat relevan dalam konteks hipertensi. Kurangnya efek signifikan pada tekanan darah, profil lipid, dan glukosa puasa mungkin mencerminkan terbatasnya ketersediaan hayati Ganodermasenyawa bioaktif, durasi uji coba yang tidak mencukupi, atau efek batas atas pada populasi dengan nilai dasar normal.
Hasil gabungan dari penelitian yang meneliti efek Ganoderma pada denyut jantung menunjukkan penurunan yang signifikan secara statistik, dengan manfaat yang terlihat pada berbagai bentuk dosis, durasi intervensi, dan karakteristik peserta. Penelitian saat ini melaporkan bahwa pada akhir periode intervensi, individu yang mengonsumsi Ganoderma tidak menunjukkan perbaikan yang signifikan secara statistik atau klinis pada penanda penyakit kronis, kadar LDL-C, atau TG di antara populasi yang sehat. Namun, suplementasi berdampak signifikan pada BMI, TC, dan MDA pada individu yang berisiko, serta pada individu yang umumnya sehat. Tidak ada efek signifikan yang diamati pada berat badan, DBP, SBP, glukosa puasa, atau HDL-C. Khususnya, suplementasi Ganoderma pada dosis di bawah 1400 mg/hari menghasilkan perbaikan signifikan pada BMI, TC, kadar kreatinin, dan MDA, sedangkan dosis yang melebihi 1400 mg/hari tidak menghasilkan perbaikan tersebut. Lebih jauh, durasi intervensi menghasilkan peningkatan signifikan pada BMI dan TC untuk peserta di bawah usia 50 tahun, sementara individu di atas 50 tahun menunjukkan perubahan nyata pada kadar kreatinin. Suplementasi Ganoderma secara positif memengaruhi MDA pada kedua kelompok usia. Studi tersebut menemukan bahwa suplementasi Ganoderma selama 8 minggu atau kurang secara signifikan meningkatkan BMI dan TC, sedangkan intervensi yang diperpanjang lebih dari 8 minggu tidak menghasilkan perubahan yang signifikan. Perbedaan gender juga diamati, dengan peningkatan yang signifikan dalam BMI dan TC di antara peserta di bawah usia 50 tahun, sementara mereka yang berusia 50 tahun ke atas menunjukkan perubahan yang nyata dalam kadar kreatinin. Selain itu, MDA dipengaruhi oleh suplementasi Ganoderma pada kedua kelompok. Tidak ada perbedaan signifikan yang terdeteksi dalam berat badan, DBP, SBP, glukosa puasa, HDL-C, LDL-C, TG, atau ALT. Kualitas metodologis yang sebagian besar buruk dari studi yang disertakan, dengan 16 dari 17 dinilai ‘Buruk’ oleh alat Cochrane Risk of Bias 2.0, menimbulkan ketidakpastian yang signifikan. Risiko bias yang tinggi dalam pengacakan, penyamaran, dan penyembunyian alokasi kemungkinan berkontribusi terhadap variabilitas dan membatasi keandalan. Heterogenitas tinggi (misalnya, I2 = 80% untuk kreatinin, 96% untuk MDA) kemungkinan muncul dari perbedaan populasi studi, protokol intervensi, dan wilayah geografis, sebagaimana dibuktikan oleh analisis subkelompok yang menunjukkan variasi regional dalam efek DBP. Temuan kami menguatkan penelitian sebelumnya yang menunjukkan bahwa suplementasi Ganoderma tidak menunjukkan efek signifikan pada BF, WC, berat, WHR, DBP, SBP, glukosa puasa, hs-CRP, TNF-α, HDL-C, LDL-C, TC, TG, ALT, AST, FRAP, dan MDA (Hu et al. 2014 ; Babamiri et al. 2022b ; Klupp et al. 2016 ; Chu et al. 2012 ).
Meta-analisis kami mengidentifikasi efek suplementasi G. lucidum yang signifikan secara statistik pada beberapa hasil, termasuk BMI (WMD = -0,43 kg/m 2 , 95% CI: -0,77 hingga -0,10, p = 0,011), kreatinin (WMD = -0,14 mg/dL, 95% CI: -0,27 hingga -0,02, p = 0,028), GPx (WMD = 2,29 U/g Hb, 95% CI: 1,67–2,92, p < 0,001), dan denyut jantung (WMD = -3,92 bpm, 95% CI: -7,45 hingga -0,40, p = 0,029). Namun, kebermaknaan klinis dari ukuran efek ini memerlukan pertimbangan yang cermat. Misalnya, pengurangan BMI (−0,43 kg/m 2 ) secara statistik signifikan tetapi sederhana, jatuh di bawah ambang batas ≥ 0,5–1 kg/m 2 yang sering dikutip sebagai relevan secara klinis untuk meningkatkan risiko kardiometabolik pada individu yang kelebihan berat badan atau obesitas (Donnelly et al. 2009 ). Demikian pula, penurunan denyut jantung (−3,92 bpm) mungkin tidak secara substansial mengubah risiko kardiovaskular pada populasi normotensi, meskipun dapat memiliki relevansi potensial pada pasien hipertensi, sambil menunggu studi lebih lanjut. Pengurangan kreatinin (−0,14 mg/dL) kecil relatif terhadap rentang referensi normal (0,6–1,2 mg/dL), yang menunjukkan dampak minimal pada fungsi ginjal, sementara peningkatan GPx (2,29 U/g Hb), enzim antioksidan, menjanjikan tetapi tidak memiliki tolok ukur yang mapan untuk signifikansi klinis dalam pengurangan stres oksidatif. Khususnya, tidak ada efek signifikan yang diamati untuk penanda kardiovaskular dan metabolik kritis seperti tekanan darah, profil lipid, atau glukosa puasa, dan kualitas bukti yang sangat rendah di semua hasil (penilaian GRADE, Tabel 4 ) menggarisbawahi ketidakpastian seputar temuan ini. Mengingat ukuran efek yang sederhana dan kualitas bukti yang sangat rendah, rekomendasi suplementasi G. lucidum masih terlalu dini. Namun, profil keamanannya dan potensi manfaatnya pada populasi tertentu (misalnya, individu yang kelebihan berat badan) menunjukkan peran sebagai terapi komplementer sambil menunggu bukti lebih lanjut.
4.2 RCT G. lucidum
Selama beberapa tahun terakhir, uji klinis yang melibatkan Ganoderma telah dilakukan untuk mengevaluasi kemanjurannya dalam mengobati berbagai gangguan. Pada tahun 1990, ekstrak G. lucidum yang larut dalam air digunakan untuk menilai efek penghambatannya pada agregasi trombosit pada pasien dengan kondisi aterosklerosis. Tingkat penghambatan agregasi trombosit maksimal berkurang secara signifikan dibandingkan dengan kelompok plasebo setelah 2 minggu pengobatan oral dengan ekstrak G. lucidum (Jun dan Ke-yan 1990 ). Namun, ekstrak ini tidak diformulasikan sebagai agen farmakologis baru untuk penyakit aterosklerosis. Penelitian telah menjelaskan potensi aplikasi terapeutik G. lucidum . Polisakarida yang berasal dari Ganoderma telah menjalani tujuh uji klinis yang membahas hepatitis B kronis, kanker paru-paru lanjut, T2DM, CHD, dan neurasthenia (Gao, Chen, et al. 2004 ; Gao et al. 2003 ; Gao, Zhou, Chen, Dai, dan Ye 2002 ; Gao, Zhou, Chen, Dai, Ye, dan Gao 2002 ; Zhou et al. 2005 ). Temuan klinis menunjukkan bahwa polisakarida dari G. lucidum ditoleransi dengan baik dan diberikan secara oral kepada pasien dengan kanker lanjut selama periode 12 minggu, tanpa efek samping yang signifikan dilaporkan (Gao, Zhou, Chen, Dai, Ye, dan Gao 2002 ). Meskipun uji klinis yang melibatkan G. lucidum tidak menghasilkan hasil yang sukses, temuan tersebut memberikan wawasan berharga untuk pengembangan obat-obatan terkait Ganoderma di masa depan, khususnya mengenai perlunya mengidentifikasi biomarker, titik akhir, dan proses farmakologis yang sesuai (Zhou et al. 2005 ). Uji coba double-blind (DB), acak (R), terkontrol plasebo (PC) yang menilai kemanjuran ekstrak air Ganoderma pada pasien dengan RA tidak berhasil; ekstrak tidak menunjukkan efek signifikan pada respons anti-inflamasi dan regulasi imun, meskipun dianggap aman dan ditoleransi dengan baik (Li et al. 2007 ). Selain itu, percobaan DB lebih lanjut yang dilakukan di Australia yang ditujukan untuk mengobati gangguan kardiovaskular pada individu dengan MetS atau diabetes tidak berhasil (Klupp et al. 2016 ). Singkatnya, disarankan bahwa ekstrak Ganoderma atau polisakarida tidak menunjukkan bioaktivitas substansial dalam studi klinis kontemporer. Investigasi terbaru menunjukkan bahwa bioaktivitas ekstrak air dari Ganoderma terkait dengan komposisi flora usus; dengan demikian, formulasi farmasi berbasis Ganoderma tetap kompleks karena jalur biologis yang rumit (Chang et al. 2015 ). Sampai saat ini, tidak ada satu pun obat-obatan terkait Ganoderma yang telah menerima persetujuan dari Badan Pengawas Obat dan Makanan Amerika Serikat (FDA), mungkin karena ambiguitas seputar bahan farmasi aktif dan mekanisme kerjanya. Antioksidan adalah agen terapeutik potensial yang dapat berkontribusi pada pencegahan aterosklerosis dan berbagai gangguan lainnya. Sejumlah penelitian in vitro dan in vivo telah menunjukkan bahwa komponen G. lucidum memiliki sifat antioksidan; namun, bukti yang mendukung efek ini pada subjek manusia masih kurang. Penelitian selanjutnya menyelidiki efek suplementasi G. lucidum pada beberapa parameter, termasuk status biomarker antioksidan dan risiko PJK. Sebuah studi intervensi DB, crossover, PC dilakukan dengan melibatkan individu yang sehat. Setelah periode pengobatan 10 hari, ada peningkatan yang diamati dalam indikator antioksidan total plasma dan perbaikan dalam biomarker yang terkait dengan PJK. Yang penting, tidak ada bukti toksisitas ginjal, hati, atau asam deoksiribonukleat (DNA) yang dicatat (Wachtel-Galor, Szeto, et al. 2004 ). Sebuah studi intervensi manusia crossover yang melibatkan tujuh individu yang sehat dilakukan untuk menilai kapasitas antioksidan G. lucidum , mengungkapkan peningkatan kekuatan antioksidan total plasma setelah dosis tunggal ekstrak G. lucidum (Wachtel-Galor et al. 2010 ). Selain itu, kemampuan antioksidan peptida polisakarida G. lucidum (PsP) dievaluasi. Sebuah uji klinis dilakukan dengan melibatkan pasien berisiko tinggi dan mereka yang memiliki angina stabil, yang menerima PsP selama 90 hari. Polisakarida menunjukkan sifat antioksidan yang signifikan dalam konteks aterosklerosis di antara kelompok berisiko tinggi dan stabil. Pasien yang diobati dengan PsP menunjukkan peningkatan kadar SOD, penurunan kadar MDA, dan pengurangan jumlah sel endotel yang bersirkulasi dan sel progenitor endotel (Sargowo et al. 2019 ). Sebuah uji coba multisenter DB, R, dilakukan untuk menilai efek dan keamanan polisakarida G. lucidum pada pasien dengan CHD. Delapan puluh delapan pasien dalam kelompok eksperimen menerima polisakarida G. lucidum selama 12 minggu. Pemberian polisakarida menghasilkan perbaikan signifikan pada hasil akhir pasien, termasuk penurunan tekanan darah dan kadar kolesterol serum (Gao, Chen, dkk. 2004 ). Penelitian lebih lanjut menunjukkan PsP yang berasal dari G. lucidum menunjukkan sifat antiinflamasi dan memberikan perlindungan pada sel endotel vaskular pada pasien dengan infark miokard elevasi ST dan infark miokard non-elevasi ST yang memiliki faktor risiko dislipidemia (Sargowo et al. 2019 ). Sebuah RCT dilakukan untuk menilai kemanjuran G. lucidum dalam mengatasi faktor risiko kardiovaskular yang terkait dengan sindrom metabolik. Hasilnya menunjukkan bahwa pemberian G. lucidum selama periode 16 minggu tidak secara signifikan mempengaruhi kadar hemoglobin A1c (HbA1c) atau glukosa plasma puasa (FPG). Lebih jauh lagi, penggunaan G. lucidum dikaitkan dengan peningkatan risiko efek samping sedang tertentu, termasuk sakit kepala, kelelahan, dan masalah gastrointestinal (Klupp et al. 2016 ). Namun, tidak ada penelitian manusia yang disebutkan di atas yang melaporkan efek samping yang signifikan, dengan demikian menyoroti G. lucidum sebagai agen terapeutik dan pencegahan yang potensial untuk berbagai CVD. Sebuah penelitian yang melibatkan 37 individu dengan risiko tinggi aterosklerosis, yang menjalani pengobatan penyakit kardiovaskular standar, menunjukkan bahwa G. lucidum PsP secara signifikan mengurangi kadar hs-CRP, IL-6, TNF-α, dan MDA (Widya et al. 2016 ). Selain itu, sebuah studi yang melibatkan 34 pasien dengan angina pektoris stabil menunjukkan bahwa pemberian PsP secara signifikan mengurangi kadar TC (Ubaidillah et al. 2016 ). Kemanjuran G. lucidum dalam CVD dinilai dalam studi prospektif, DB, PC. Delapan puluh empat relawan yang didiagnosis dengan T2DM dan MetS menerima suplemen G. lucidum , atau G. lucidum yang dikombinasikan dengan Cordyceps sinensis, atau plasebo untuk mengatasi faktor risiko kardiovaskular. Hasil studi menunjukkan bahwa G. lucidum tidak memberikan keuntungan signifikan dalam pencegahan CVD di antara individu dengan MetS (Klupp et al. 2016 ). Analisis dari lima studi yang mencakup 398 partisipan menunjukkan bahwa G. lucidum tidak efektif dalam pengobatan tekanan darah tinggi (Klupp et al. 2015 ). Secara kolektif, temuan ini menunjukkan bahwa G. lucidum paling efektif dalam memberikan perlindungan kardiovaskular bila digunakan bersama dengan obat kardiovaskular. Lebih jauh lagi, obat-obatan Ganoderma telah digunakan baik sebagai monoterapi maupun dalam kombinasi dengan senyawa lain atau agen kemoterapi dalam studi klinis. Akan tetapi, komposisi obat-obatan Ganoderma prospektif ini masih kompleks dan memerlukan penyelidikan lebih lanjut. Kompleksitas ini menghadirkan tantangan signifikan untuk uji klinis, yang harus dilakukan sesuai dengan pedoman FDA tentang Kimia, Manufaktur, dan Kontrol (CMC) untuk studi klinis. Akibatnya, bahan farmasi aktif (API) yang transparan untuk obat-obatan kandidat sangat penting untuk penyelidikan klinis Ganoderma di masa mendatang. Tinjauan sistematis mengungkap keterbatasan metodologis yang signifikan di seluruh RCT yang disertakan yang secara fundamental mengkompromikan keandalan dan generalisasi temuan. Pemeriksaan kritis terhadap tabel penilaian kualitas studi mengungkap kerentanan metodologis yang meluas: mayoritas studi (16 dari 17) dinilai sebagai kualitas “Buruk”, dengan hanya satu studi yang mencapai peringkat “Cukup”. Kekurangan metodologis yang paling menonjol meliputi pendekatan yang tidak konsisten dan seringkali tidak memadai untuk pengacakan, penyembunyian alokasi, dan penyamaran. Secara khusus, banyak studi menunjukkan domain yang tidak jelas (U) atau berisiko tinggi (H) di area metodologis penting seperti pembuatan urutan acak dan penyembunyian alokasi. Proses penyamaran khususnya bermasalah, dengan banyak studi menunjukkan penyamaran yang tidak lengkap atau tidak jelas dari peserta, personel, dan penilai hasil—kelemahan kritis yang memperkenalkan potensi signifikan untuk bias kinerja dan deteksi. Konsentrasi geografis penelitian menghadirkan kendala metodologis substansial lainnya, dengan 12 dari 17 penelitian dilakukan di negara-negara Asia Timur, terutama di Tiongkok, Hong Kong, dan Taiwan. Homogenitas geografis ini sangat membatasi validitas eksternal dan generalisasi temuan ke berbagai populasi dengan konteks genetik, pola makan, dan lingkungan yang berbeda. Lebih jauh, penelitian menunjukkan heterogenitas yang nyata dalam protokol intervensi, termasuk variasi substansial dalam dosis G. lucidum (berkisar dari 225 hingga 11.200 mg/hari), formulasi suplemen, dan durasi uji coba (1–24 minggu). Ukuran sampel secara konsisten kecil, dengan sebagian besar penelitian melibatkan kurang dari 100 peserta, yang selanjutnya mengurangi kekuatan statistik dan keandalan hasil. Dominasi uji coba durasi pendek membatasi kesimpulan yang berarti tentang efek jangka panjang, sementara kurangnya standardisasi dalam persiapan G. lucidum —termasuk variasi dalam metode ekstraksi, konsentrasi senyawa aktif, dan jenis suplemen—memperkenalkan lapisan tambahan kompleksitas metodologis dan potensi bias. Kelemahan metodologi sistemik ini menggarisbawahi kebutuhan mendesak akan penelitian yang lebih ketat, terstandarisasi, dan metodologi yang kuat untuk secara definitif menetapkan signifikansi klinis suplementasi G. lucidum .
4.3 Model Hewan untuk Evaluasi G. lucidum
Tinjauan ini mengindikasikan bahwa mayoritas studi praklinis yang melibatkan Ganoderma berfokus pada model hewan daripada subjek manusia. Sifat kardioprotektif ekstrak G. lucidum diselidiki melalui penerapan iskemia global dan reperfusi pada jantung tikus yang diisolasi dan diperfusi. Dalam studi ini, ekstrak G. lucidum diberikan secara profilaksis kepada tikus selama periode 15 hari. Intervensi ini ditemukan untuk mencegah kematian nekrotik kardiomiosit tikus dan mengurangi kontraktur reperfusi (Lasukova et al. 2015 ). Yang penting, pemberian ekstrak G. lucidum diamati untuk meringankan disfungsi diastolik dan mencegah kerusakan ireversibel pada kardiomiosit (Lasukova et al. 2008 ). Diabetes melitus, gangguan metabolik, dikaitkan dengan peningkatan kejadian CVD, terutama karena kerusakan arteri yang diakibatkan oleh peningkatan kadar glukosa darah (Klein et al. 2002 ; Fox et al. 2008 ; Shah et al. 2008 ). Akibatnya, suplemen yang mendukung manajemen diabetes dapat secara signifikan mengurangi risiko CVD. Dalam sebuah penelitian, 35 tikus diberikan suplemen polisakarida yang berasal dari ekstrak G. lucidum , yang memfasilitasi proses penyembuhan endotel. Hasilnya menunjukkan bahwa terapi polisakarida memperbaiki kerusakan vaskular pada model tikus ini (Heriansyah et al. 2019 ). Diet kaya lipid diakui sebagai faktor risiko yang signifikan untuk timbulnya CVD (Fleming 2002 ), dan penurunan berat badan merupakan strategi penting untuk mencegah CVD pada individu dengan obesitas (Sowers 2003 ). Ekstrak air G. lucidum telah terbukti mengurangi berat badan, peradangan, dan resistensi insulin pada tikus yang diberi diet tinggi lemak (HFD) (Chang et al. 2015 ). Dalam uji coba terpisah, spora Ganoderma diberikan secara oral selama 4 minggu kepada tikus jantan dewasa. Spora ini mengurangi TC dan TG pada tikus diabetes dan mengurangi tingkat stres oksidatif; khususnya, terdapat peningkatan regulasi gen yang terkait dengan metabolisme lipid, khususnya asil-CoA oksidase 1 (ACOX1), asetil-CoA karboksilase (ACC), dan ekspresi gen Insig-1/2. ACOX1 diaktifkan lebih dari lima kali lipat pada tikus diabetes yang diobati dengan spora, yang menunjukkan peningkatan beta-oksidasi lipid pada subjek ini (Wang et al. 2014 ). Dislipidemia merupakan faktor risiko signifikan untuk CVD (Miller 2009 ). Dalam penyelidikan hewan percobaan, G. lucidum telah menunjukkan efek anti-hiperlipidemia dengan menurunkan kadar plasma TC, LDL-C, dan TG (Chen et al. 2005 ). Radikal bebas hidrogen peroksida sering meningkat dalam konteks dislipidemia, sehingga meningkatkan risiko aterosklerosis; akibatnya, antioksidan sangat penting untuk mencegah kerusakan vaskular. Penelitian yang melibatkan tikus dengan diet tinggi kolesterol yang disuplemen dengan 50, 150, dan 300 mg/kg berat badan PsP yang berasal dari G. lucidum menunjukkan bahwa PsP bertindak sebagai antioksidan yang kuat. Lebih jauh, PsP dapat menghambat aterogenesis yang terkait dengan dislipidemia, dengan dosis optimal diidentifikasi sebagai 300 mg/kg berat badan (Wihastuti dan Heriansyah 2017 ). Studi tambahan menunjukkan bahwa polisakarida yang diekstraksi dari G. lucidum secara signifikan mengurangi penambahan berat badan pada tikus yang mengalami HFD, menggarisbawahi peran potensialnya sebagai agen hipolipidemik. Selain itu, ia menunjukkan sifat antioksidan dan antiapoptotik pada tikus yang diberi HFD (Liang et al. 2018 ). Sebuah penelitian yang melibatkan tikus hipertensi jantan dewasa mengungkapkan bahwa pemberian ekstrak air dari G. lucidum selama 7 minggu menghasilkan penurunan tekanan darah yang sebanding dengan yang diamati pada tikus yang diobati dengan losartan, antagonis reseptor angiotensin II (Shevelev et al. 2018 ).
4.4 Pendekatan Masa Depan dalam RCT G. lucidum
Lima belas studi klinis yang melibatkan Ganoderma telah didaftarkan; namun, hanya lima yang saat ini sedang berlangsung, dengan mayoritas tidak merekrut peserta atau memiliki status yang tidak ditentukan. Lima uji klinis yang sedang berlangsung berfokus pada kondisi seperti eksim, uveitis, kanker prostat, kanker paru-paru, kanker payudara, kanker gastrointestinal, dan penyakit Parkinson. Tabel S3 memberikan informasi terperinci mengenai status perekrutan dan status studi klinis yang tidak diketahui. Pembaruan terkini mengenai kuantitas dan kualitas uji klinis gagal menjelaskan penerapan Ganoderma yang disengaja pada gangguan yang ditentukan. Meskipun beberapa uji klinis ada, ukuran sampel, standar, prosedur, dan kriteria yang digunakan tidak cukup untuk memenuhi tolok ukur yang ditetapkan oleh berbagai skala penilaian (Berger dan Alperson 2009 ). Ada variabilitas yang signifikan dalam desain uji coba, dengan mayoritas bersifat pendahuluan (Fase I/II), yang terutama dilakukan untuk menilai keamanan dan pemilihan rentang dosis untuk studi lanjutan yang potensial. Para penulis menganjurkan evaluasi yang lebih ketat, seperti yang ditunjukkan dalam kualitas uji klinis yang melibatkan produk alami dalam penelitian kanker (Ahmad 2020 ), yang dapat memberikan wawasan berharga untuk studi klinis di masa mendatang. Studi lanjutan (Fase III/IV) yang menggunakan metodologi sistematis, pemantauan berbasis risiko, ukuran sampel yang lebih besar, kriteria inklusi dan eksklusi yang tepat, standar yang ditetapkan, penyamaran, pengacakan, protokol putus sekolah, dan uji coba multisenter sangat penting. Data literatur yang komprehensif sangat penting untuk mendukung penggunaan Ganoderma bersama dengan berbagai makanan, minuman, atau herbal yang dapat menghambat atau mensinergikan efeknya melalui mekanisme yang memengaruhi penyerapan, bioavailabilitas, ekskresi, atau pembentukan kompleks karena adanya serat dalam produk tertentu. Makanan dan minuman yang paling sering dikonsumsi telah dikaitkan dengan interaksi yang dilaporkan (Bushra et al. 2011 ). Beberapa produk yang berasal dari Ganoderma tersedia di pasaran, termasuk sirup, bubuk, dan kapsul. Sementara produk-produk ini dapat menentukan kuantitas komponen aktif dalam dosis yang dianjurkan, lokasi geografis dapat dipengaruhi oleh faktor-faktor yang disebutkan di atas. Variabilitas dalam karakteristik sampel dapat memengaruhi kualitas dan kuantitas mikokimia dalam Ganoderma, dengan demikian memengaruhi kandungan obat aktif dalam dosis tertentu dan selanjutnya khasiat obat dari produk akhir. Sangat penting untuk menilai dan menjaga konsistensi dalam kualitas sampel Ganoderma sesuai dengan variasi lokal. Ini dapat dicapai secara efektif dengan mematuhi standar WHO untuk penilaian dan pemeliharaan kualitas produk herbal (WHO G 2007 ). Temuan dapat divalidasi dengan kuat menggunakan model praklinis diikuti oleh studi klinis yang ketat. Penggabungan nanopartikel (NP) bersama dengan Ganoderma merupakan pendekatan inovatif dalam terapi herbal yang ditujukan untuk meningkatkan khasiat terapeutik, mengurangi frekuensi pemberian, dan meminimalkan efek samping atau toksisitas. Obat herbal atau ekstrak sering kali tidak larut atau memiliki kelarutan terbatas, yang berpotensi menyebabkan penurunan penyerapan, bioavailabilitas, dan kemanjuran terapeutik. NP, termasuk NP polimerik, nanoemulsi, liposom, nanogel, dan NP lipid padat, menawarkan keuntungan dalam mengubah dan memanfaatkan obat dengan sifat terapeutik suboptimal dengan meningkatkan kelarutan, bioavailabilitas, dan metode pengiriman yang ditargetkan (Ansari et al. 2012 ). Penelitian komprehensif diperlukan untuk ekstrak, bubuk, sirup, kapsul, dan senyawa aktif Ganoderma yang diisolasi untuk menetapkannya sebagai kandidat pengobatan yang layak dengan atribut terapeutik dan tertarget yang ditingkatkan pada dosis minimal dan toksisitas yang berkurang. Seiring meningkatnya kesadaran akan perawatan kesehatan, produk-produk terkait Ganoderma telah menarik perhatian signifikan karena bukti ilmiah substansial yang mendukung manfaat kesehatannya, termasuk regulasi mikrobiota usus, imunomodulasi, dan neuroproteksi (Chang et al. 2015 ; Gokce et al. 2015 ). Selain itu, asam ganoderat dan β-glukan telah diakui kontribusinya terhadap keuntungan kesehatan Ganoderma (Ferreira et al. 2015 ; Wu et al. 2013 ). Berbagai metodologi untuk produksi metabolit bermanfaat ini telah diidentifikasi; oleh karena itu, nutraseutika Ganoderma dikembangkan dengan baik. Meskipun Ganoderma secara luas diakui sebagai jamur obat, uji klinis yang melibatkan Ganoderma secara konsisten gagal selama beberapa dekade terakhir. Meskipun Ganoderma spp. menunjukkan banyak sifat farmakologis dalam penelitian ilmiah, terdapat perbedaan yang signifikan antara aplikasi nutraseutika dan farmasi. Kompleksitas formulasi, komponen aktif yang tidak jelas, dan mekanisme biologis telah mengakibatkan kegagalan farmasi berbasis Ganoderma dalam uji klinis. Oleh karena itu, penggambaran berbagai bahan aktif farmasi dan efek farmakologisnya sangat penting untuk kemajuan pengobatan yang berasal dari Ganoderma. Fitur penting dari meta-analisis ini adalah heterogenitas tinggi yang diamati dalam hasil tertentu, seperti hs-CRP ( I 2 = 91,9%), TNF-α ( I 2 = 89,9%), dan DBP ( I 2 = 74,0%), yang memerlukan pertimbangan sumber-sumber yang mendasarinya. Analisis subkelompok kami mengungkapkan bahwa faktor-faktor seperti kondisi kesehatan, wilayah geografis, dan ukuran sampel dapat berkontribusi terhadap variabilitas ini. Misalnya, efek DBP bervariasi secara signifikan menurut wilayah ( p = 0,013), dengan pengurangan yang lebih kuat di Amerika/Oseania/Eropa (WMD = −5,20, p = 0,001) dibandingkan dengan Asia Timur (WMD = 0,67, p = 0,884, I 2 = 80,0%), yang berpotensi mencerminkan perbedaan dalam pola diet, profil genetik, atau ketelitian desain penelitian. Demikian pula, heterogenitas yang menonjol dalam penanda inflamasi kemungkinan berasal dari keragaman klinis—serta tingkat inflamasi dasar—dan faktor metodologis, termasuk sensitivitas uji dan waktu pengukuran, seperti yang terlihat dalam penelitian nutraseutika sebelumnya (Jafari et al. 2024 ; Jafari et al. 2025 ). Analisis sensitivitas lebih lanjut menyoroti pengaruh studi individual, seperti Klupp et al. ( 2016 ) pada kolesterol total ( I 2 berkurang pasca-eksklusi), yang menggarisbawahi peran karakteristik uji coba tertentu. Dengan menggunakan model efek acak dan stratifikasi subkelompok yang komprehensif, kami memperhitungkan variabilitas ini, memastikan estimasi gabungan yang kuat. Temuan-temuan ini tidak hanya mengontekstualisasikan potensi terapeutik Ganoderma lucidum tetapi juga menyoroti kompleksitas efeknya di berbagai populasi, menawarkan batu loncatan untuk penelitian masa depan dalam intervensi nutrisi yang dipersonalisasi. 4.5 Kekuatan dan Keterbatasan Tinjauan sistematis dan meta-analisis ini merupakan upaya perintis untuk menilai efek klinis suplementasi G. lucidum pada beragam indeks terkait kesehatan. Dengan menggunakan pedoman PRISMA dan kerangka kerja GRADE, studi ini memastikan transparansi dan ketelitian metodologis, menyediakan sintesis bukti terkini yang kuat. Dimasukkannya berbagai hasil kesehatan, seperti penanda stres oksidatif, biomarker inflamasi, dan profil lipid, menawarkan wawasan komprehensif tentang potensi aplikasi terapeutik G. lucidum . Analisis subkelompok dan evaluasi dosis-respons semakin memperkaya temuan, mengungkap hubungan bernuansa antara dosis suplementasi, durasi, dan hasil kesehatan. Khususnya, analisis ini menggabungkan berbagai studi mengenai berbagai kondisi kesehatan, termasuk asma, artritis reumatoid, dan gangguan metabolik, sehingga memperluas penerapan klinisnya. Selain itu, eksplorasi mekanisme biologis yang masuk akal—seperti jalur antioksidan dan anti-inflamasi—meningkatkan nilai translasi temuan. Akan tetapi, penelitian ini bukannya tanpa keterbatasan. Ukuran sampel yang kecil dalam beberapa uji coba yang disertakan dan heterogenitas dalam desain penelitian, bentuk suplementasi, dan ukuran hasil mengurangi kekuatan bukti secara keseluruhan. Sebagian besar uji coba dilakukan di Asia Timur, yang dapat membatasi generalisasi temuan pada populasi dengan konteks diet, genetik, dan lingkungan yang berbeda. Selain itu, dominasi penelitian berdurasi pendek membatasi kesimpulan tentang efek jangka panjang. Penilaian GRADE mengungkapkan dominasi bukti berkualitas rendah atau sangat rendah untuk banyak hasil, yang menyoroti perlunya uji coba yang dirancang lebih baik untuk memperkuat kepercayaan pada temuan. Selain itu, variabilitas dalam kualitas dan standarisasi produk G. lucidum di seluruh penelitian menimbulkan potensi bias. Penilaian GRADE mengungkap tantangan metodologi kritis yang secara fundamental merusak kepastian bukti di semua hasil. Kualitas bukti yang “sangat rendah” yang dominan berasal dari beberapa faktor yang saling berhubungan: sebagian besar studi (> 50%) menunjukkan risiko bias yang tinggi, yang secara signifikan membatasi keandalan hasil yang dilaporkan. Ketidakkonsistenan metodologi terbukti melalui heterogenitas yang tinggi ( I 2 > 50%) dalam beberapa hasil, yang menunjukkan variabilitas substansial dalam desain studi, protokol intervensi, dan karakteristik populasi. Ketidaktepatan lebih lanjut membahayakan kualitas bukti, dengan sebagian besar analisis mencakup kurang dari 400 peserta dan interval kepercayaan sering kali melewati ambang signifikansi statistik. Ketidaklangsungan diperkenalkan oleh konsentrasi geografis studi, terutama dalam konteks Asia Timur, yang berpotensi membatasi generalisasi temuan. Interval kepercayaan yang sempit dan penurunan sistematis di seluruh domain mencerminkan keterbatasan saat ini dalam metodologi penelitian seputar suplementasi G. lucidum . Keterbatasan metodologi ini mengharuskan penafsiran hasil yang cermat dan menggarisbawahi kebutuhan mendesak akan uji coba terkontrol acak berskala besar dan metodologis yang kuat yang dapat memberikan bukti yang lebih pasti mengenai efek klinis G. lucidum .
Keterbatasan tambahan adalah tidak adanya meta-regresi untuk lebih jauh mengeksplorasi sumber heterogenitas yang diamati di seluruh hasil. Sesuai dengan Cochrane Handbook for Systematic Reviews of Interventions (Higgins 2008 ), meta-regresi tidak direkomendasikan ketika kurang dari 10 studi tersedia per kovariat karena kekuatan statistik yang tidak memadai dan risiko overfitting, yang dapat menghasilkan hasil yang tidak dapat diandalkan. Dalam analisis kami, jumlah studi per hasil berkisar antara 3 hingga 9, berada di bawah ambang batas ini untuk semua variabel. Akibatnya, kami mengandalkan analisis subkelompok yang dikelompokkan berdasarkan faktor-faktor seperti kondisi kesehatan, dosis, dan durasi untuk menyelidiki heterogenitas, pendekatan yang lebih layak mengingat terbatasnya jumlah studi. Sementara pilihan ini sejalan dengan pedoman yang ditetapkan, hal itu membatasi kemampuan kami untuk secara bersamaan menilai berbagai sumber variabilitas, keterbatasan yang dapat diatasi dalam meta-analisis masa depan dengan kumpulan data yang lebih besar.
Untuk mengatasi keterbatasan yang diidentifikasi dalam tinjauan ini, penelitian di masa mendatang harus memprioritaskan uji coba terandomisasi skala besar dan multisenter yang melibatkan beragam populasi di berbagai konteks geografis dan budaya. Uji coba ini harus menggunakan metodologi standar untuk protokol intervensi, pengukuran hasil, dan standar pelaporan guna memastikan keterbandingan dan reproduktifitas. Evaluasi keamanan dan kemanjuran jangka panjang G. lucidum melalui periode tindak lanjut yang diperpanjang sangat penting untuk memahami perannya dalam manajemen penyakit kronis.
Penelitian lebih lanjut harus difokuskan pada penjelasan mekanisme yang mendasari manfaat kesehatan G. lucidum dengan menggabungkan analisis biomarker dan teknik molekuler tingkat lanjut. Uji coba yang menyelidiki interaksi sinergis atau antagonis antara G. lucidum dan komponen makanan, herbal, atau obat-obatan lainnya sangat penting untuk mengoptimalkan penggunaannya dalam praktik klinis. Penyertaan metode analisis tingkat lanjut, seperti formulasi berbasis NP, dapat meningkatkan bioavailabilitas dan potensi terapeutik G. lucidum , yang membuka jalan bagi aplikasi inovatif dalam pengobatan integratif.
Akhirnya, standardisasi produk G. lucidum dalam hal kandungan senyawa aktif, kualitas, dan konsistensi harus diprioritaskan. Kerangka kerja regulasi, seperti pedoman WHO untuk obat-obatan herbal, dapat memberikan dasar untuk memastikan keandalan dan keamanan produk-produk ini dalam pengaturan klinis. Dengan mengatasi kesenjangan penelitian ini, studi masa depan dapat secara signifikan memajukan pemahaman kita tentang potensi terapeutik G. lucidum dan menginformasikan rekomendasi berbasis bukti untuk penggunaannya dalam promosi kesehatan dan manajemen penyakit. Keterbatasannya mencakup heterogenitas yang tinggi dalam hasil (misalnya, I2 = 96% untuk MDA), ukuran sampel yang kecil (sebagian besar studi <100 peserta), dan variabilitas dalam sediaan Ganoderma (misalnya, ekstrak vs. bubuk spora), yang memperkenalkan potensi bias dan membatasi komparabilitas. Konsentrasi geografis studi di Asia Timur membatasi generalisasi. Tidak adanya meta-regresi, karena studi per hasil yang tidak mencukupi, membatasi eksplorasi sumber heterogenitas.
5 Kesimpulan
Tinjauan sistematis dan meta-analisis ini menyoroti potensi manfaat suplementasi G. lucidum dalam meningkatkan indeks terkait kesehatan utama, khususnya BMI, kadar kreatinin, aktivitas GPx, dan HR. Meskipun dampaknya minimal pada parameter kardiometabolik lainnya, temuan tersebut menggarisbawahi potensinya sebagai terapi komplementer untuk mengelola faktor risiko tertentu yang terkait dengan penyakit kardiovaskular dan metabolik. Dengan keamanan dan aksesibilitasnya yang baik, G. lucidum dapat dipertimbangkan dalam strategi diet dan terapi. Penelitian di masa mendatang harus memprioritaskan uji klinis yang dirancang dengan baik untuk mengeksplorasi kemanjuran jangka panjang, dosis dan formulasi yang optimal, serta mekanisme yang mendasarinya. Ganoderma lucidum mungkin memiliki efek sederhana pada BMI, kreatinin, GPx, dan detak jantung, tetapi kualitas bukti yang sangat rendah menghalangi rekomendasi yang kuat. RCT yang dirancang dengan baik diperlukan untuk mengonfirmasi kemanjuran dan relevansi klinisnya.

